题目内容
15.金属钛晶胞结构如图所示,设钛原子的半径为r,则该晶胞体积的表达式为8r3
分析 金属钛为六方最密堆积的结构,求出a(晶胞的长)、b(晶胞的宽)、c(晶胞的高),即可求出晶胞体积.
解答 解:a(晶胞的长)=b(晶胞的宽)=2r.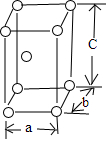
c(晶胞的高)=$\frac{4}{3}$$\sqrt{6}$r.
V(晶胞的体积)=abcSin120°=(2r)2×$\frac{4}{3}$$\sqrt{6}$r×$\frac{\sqrt{3}}{2}$=8r3,故答案为:8r3.
点评 本题考查金属晶体堆积模型,为高频考点,侧重考查学生分析及空间想象能力,难点是晶体的体积计算.

练习册系列答案
相关题目
5.某科研小组设计出利用工业废酸(含10%的H2SO4)和废弃氧化铜锌矿制取活性ZnO的方案如图.
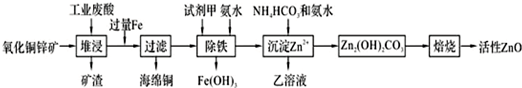
已知:298K时各离子开始沉淀及完全沉淀时的pH如表所示.
请回答下列问题:
(1)在H2SO4作用下矿石中含有的ZnS溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)<Ksp(ZnS)(选填“>”、“<”或“=”).
(2)除铁过程中试剂甲最好选用B(填序号).
A.KMnO4 B.H2O2 C.HNO3 D.Cl2
(3)除铁过程中加入氨水的目的是调节pH在3.2~6.2范围之间.
(4)试写出沉淀Zn2+时发生反应的离子方程式:2Zn2++3NH3?H2O+HCO3-=Zn2(OH)2CO3↓+3NH4++H2O.

已知:298K时各离子开始沉淀及完全沉淀时的pH如表所示.
| 离子 | 开始沉淀时的pH | 完全沉淀时的pH |
| Fe2+ | 6.34 | 9.7 |
| Fe3+ | 1.48 | 3.2 |
| Zn2+ | 6.2 | 8.0 |
(1)在H2SO4作用下矿石中含有的ZnS溶解而CuS不溶,这是由于相同温度下:Ksp(CuS)<Ksp(ZnS)(选填“>”、“<”或“=”).
(2)除铁过程中试剂甲最好选用B(填序号).
A.KMnO4 B.H2O2 C.HNO3 D.Cl2
(3)除铁过程中加入氨水的目的是调节pH在3.2~6.2范围之间.
(4)试写出沉淀Zn2+时发生反应的离子方程式:2Zn2++3NH3?H2O+HCO3-=Zn2(OH)2CO3↓+3NH4++H2O.
6.一定条件下反应:2SO2+O2?2SO3 发生时,能使V(SO2)增大的措施有( )
①增大压强 ②降低压强 ③通入SO2 ④增加的O2量 ⑤升高温度 ⑥降低温度.
①增大压强 ②降低压强 ③通入SO2 ④增加的O2量 ⑤升高温度 ⑥降低温度.
| A. | ①②③⑤ | B. | ②③④⑥ | C. | ②③④⑤ | D. | ①③④⑤ |
3.C、N、S元素都是生命体的重要组成元素,它们在自然界的平衡已受到较大的破坏.C、N、S元素在地球大气圈、岩石圈、水系、生物圈等的循环过程中会产生的物质是( )
①HNO3 ②CO2 ③糖类 ④CH4 ⑤SO2.
①HNO3 ②CO2 ③糖类 ④CH4 ⑤SO2.
| A. | ①②③④⑤ | B. | ②③⑤ | C. | ②③④ | D. | ② |
20.下列离子方程式正确的是( )
| A. | 少量金属钠溶解在AlCl3溶液中:2Na+2H2O=2Na++H2↑ | |
| B. | 铝溶解在NaOH溶液中:2Al+2OH-+2H2O=2AlO2-+3H2↑ | |
| C. | MgO溶于醋酸中:MgO+2H+=H2O+Mg2+ | |
| D. | Al(OH)3溶于稀硫酸中:OH-+H+=H2O |
5.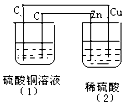 如图的装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过了0.02mole-.若不考虑溶液体积的变化,下列叙述正确的( )
如图的装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过了0.02mole-.若不考虑溶液体积的变化,下列叙述正确的( )
 如图的装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过了0.02mole-.若不考虑溶液体积的变化,下列叙述正确的( )
如图的装置中,溶液的体积均为200mL,开始时电解质溶液的浓度均为0.1mol/L,工作一段时间后,测得导线上通过了0.02mole-.若不考虑溶液体积的变化,下列叙述正确的( )| A. | 相同条件下,两容器产生的气体体积相同 | |
| B. | (1)、(2)溶液的pH值均减小 | |
| C. | (1)中阳极电极反应方程式为:4OH--4e-═2H2O+O2↑ | |
| D. | (2)中正极反应为Zn-2e-═Zn2+ |
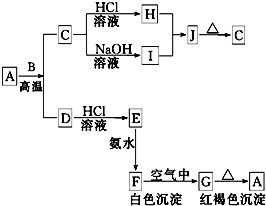 A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.
A是一种红棕色金属氧化物,B、D是金属单质,J是一种难溶于水的白色化合物,受热后容易发生分解.