题目内容
8.乙酸橙花酯是一种食用香料,其结构简式如图,下列有关叙述错误的是( )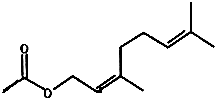
| A. | 分子式为C12H20O2 | |
| B. | 它的同分异构体中不可能有酚类 | |
| C. | 其一氯化物共7种 | |
| D. | 1mol该有机物与1mol水在一定条件下反应可能的产物有6种 |
分析 A.根据结构简式确定分子式;
B.分子中含有3个双键,则不饱和度为3,而酚类物质的不饱和度为4;
C.该分子中H原子有8种;
D.碳碳双键能发生加成反应,酯基能发生水解反应.
解答 解:A.根据结构简式确定分子式为C12H20O2,故A正确;
B.分子中含有3个双键,则不饱和度为3,而酚类物质的不饱和度为4,则它的同分异构体中不可能有酚类,故B正确;
C.该分子中H原子有8种,所以其一氯代物有8种,故C错误;
D.碳碳双键能发生加成反应,酯基能发生水解反应,所以1mol该有机物与1mol水在一定条件下反应可能的产物有6种,故D正确;
故选C.
点评 本题考查有机物结构和性质,为高频考点,明确官能团及其性质关系是解本题关键,侧重考查学生分析判断能力,易错选项是B,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
18.今年11月初经历了辽宁史上最严重的雾霾天气,作为雾霾的重要污染源之一,秸秆焚烧问题引起了大家更多的关注.我省桓仁县的“秸秆变燃气”工程实现了秸秆的无污染利用.下列说法不正确的是( )
| A. | 霾的形成与PM2.5有直接关系 | |
| B. | 煤的氧化和秸秆变燃气本质上都是提供热量使原料气体,是物理变化 | |
| C. | 大量秸焚烧秆可能是导致霾的形成主要是因为不完全燃烧生成大量的固体颗粒 | |
| D. | 秸秆变燃气,燃烧效率高,产物无污染,有利于保护环境 |
19.下列说法正确的是( )
| A. | 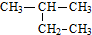 与 与 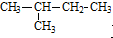 互为同分异构体 互为同分异构体 | |
| B. | 红磷与白磷互为同素异形体 | |
| C. | CH3CH2OH与HOCH2CH2CH2OH互为同系物 | |
| D. | 35Cl与37Cl为同一种核素 |
16.下列各组离子在pH=1的溶液中,因发生氧化还原反应而不能大量共存的是( )
| A. | Na+、K+、CO32-、NO3- | B. | NH4+、Na+、SO42-、S2- | ||
| C. | Al3+、Na+、NO3-、I- | D. | CH3COO-、Cl-、Na+、NH4+ |
13.有机物M和N都是临床上常用的止血药,其结构如图: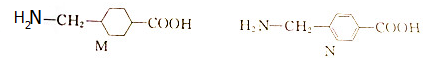
下列说法正确的是( )
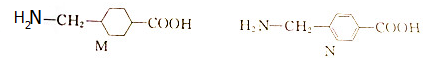
下列说法正确的是( )
| A. | 1mol M完全燃烧生成6.5mol H2O | B. | CH3CH2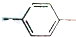 NO2与N互为同分异构体 NO2与N互为同分异构体 | ||
| C. | M、N分子中所有碳原子均共平面 | D. | M、N的核磁共振氢谱均只有5个峰 |
7.氢能是一种洁净的可再生能源,制备和储存氢气是氢能开发的两个关键环节.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
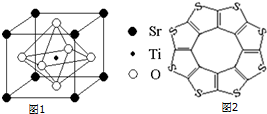
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.
Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
从表中数据可以看出,C16S8中碳硫键键长介于C-S与C═S之间,原因可能是:分子中的C与S原子之间有π键或分子中的碳硫键具有一定程度的双键性质.
④C16S8与H2微粒间的作用力是范德华力.
Ⅰ氢气的制取
(1)水是制取氢气的常见原料,下列说法正确的是AB(填序号).
A.H3O+的空间构型为三角锥形
B.水的沸点比硫化氢高
C.冰晶体中,1mol水分子可形成4mol氢键
(2)科研人员研究出以钛酸锶为电极的光化学电池,用紫外线照射钛酸锶电极,使水分解产生氢气.已知钛酸锶晶胞结构如图1,则其化学式为SrTiO3.

Ⅱ氢气的存储
(3)Ti(BH4)2是一种储氢材料.
①Ti原子在基态时的核外电子排布式是1s22s22p63s23p63d24s2或[Ar]3d24s2.
②Ti(BH4)2可由TiCl4和LiBH4反应制得,TiCl4 熔点-25.0℃,沸点136.94℃,常温下是无色液体,则TiCl4晶体类型为分子晶体.
(4)最近尼赫鲁先进科学研究中心借助ADF软件对一种新型环烯类储氢材料(C16S8)进行研究,从理论角度证明这种分子中的原子都处于同一平面上(结构如图2所示),每个平面上下两侧最多可储存10个H2分子.
①元素电负性大小关系是:C<S(填“>”、“=”或“<”).
②分子中C原子的杂化轨道类型为sp2.
③有关键长数据如下:
| C-S | C═S | C16S8中碳硫键 | |
| 键长/pm | 181 | 155 | 176 |
④C16S8与H2微粒间的作用力是范德华力.
4.下列说法不合理的是( )
| A. | 在稀硫酸中加入铜粉,铜粉不溶解,若加入KNO3固体,铜粉溶解 | |
| B. | “溶洞”的形成过程中发生了碳酸钙与水、CO2的反应 | |
| C. | 采用催化转化技术可以将汽车尾气中的氮氧化物CO转化为无毒气体 | |
| D. | FeCl3、Na2O2、CuS均可由相应的单质直接化合而成 |
5.对于图象①→④的辨析正确的是( )
| A. | 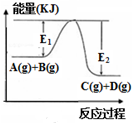 表示反应A(g)+B(g)→C(g)+D(g)是吸热反应,吸收能量(E2-E1)kJ | |
| B. | 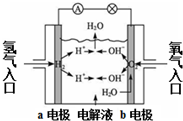 为氢氧燃料电池示意图,正、负极通入的气体体积之比为2:1 | |
| C. | 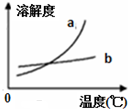 是物质a、b的溶解度曲线,可以用重结晶法从a、b混合物中提纯a | |
| D. | 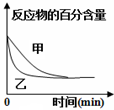 可表示压强对反应2A(g)+B(g)?3C(g)+D(s)的影响,且乙的压强大 |
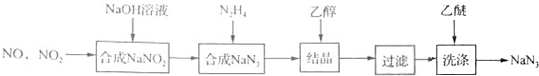
 .
.