题目内容
15.下列说法错误的是( )| A. | 碳酸钠固体中含有碳酸氢钠固体,可用灼烧的方法 | |
| B. | 用酚酞溶液可以鉴别饱和食盐水和饱和纯碱溶液 | |
| C. | 25℃,碳酸氢钠在水中的溶解度比碳酸钠的大 | |
| D. | 氢氧化钠与二氧化碳的反应与量有关 |
分析 A.碳酸氢钠不稳定,加热易分解;
B.纯碱溶液呈碱性;
C.碳酸氢钠的溶解度比碳酸钠小;
D.氢氧化钠与二氧化碳的反应可生成碳酸钠、碳酸氢钠.
解答 解:A.碳酸氢钠不稳定,加热易分解,可用灼烧的方法除杂,故A正确;
B.纯碱为强碱若酸盐,溶液呈碱性,可用酚酞溶液鉴别,故B正确;
C.相同温度下,碳酸氢钠的溶解度比碳酸钠小,故C错误;
D.氢氧化钠与二氧化碳的反应可生成碳酸钠、碳酸氢钠,涉及离子方程式为CO2+2OH-=H2O+CO32-、CO2+OH-=HCO3-,故D正确.
故选C.
点评 本题考查钠的化合物,为高频考点,侧重于学生的分析能力和元素化合物知识的综合理解和运用的考查,注意把握相关基础知识的积累,难度不大.

练习册系列答案
 名师导航单元期末冲刺100分系列答案
名师导航单元期末冲刺100分系列答案 名校名卷单元同步训练测试题系列答案
名校名卷单元同步训练测试题系列答案
相关题目
5.0.02mol•L-1的HCN溶液与0.02mol•L-1的NaCN溶液等体积混合,已知混合液中[CN-]<[Na+],则下列关系正确的是( )
| A. | c(Na+)>c(CN-)>c(OH-)>c(H+) | B. | c(HCN)+(CN-)=0.04 mol•L-1 | ||
| C. | c(Na+)+c (OH-)=c(CN-)+c(H+) | D. | c(CN-)>c(HCN) |
6.A、B、C三种强电解质,它们在水中电离出的离子如表所示:
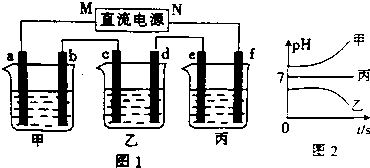
如图1中,甲、乙、丙三个烧杯依次分别盛放足量的A溶液、足量的B溶液、足量的C溶液,电极均为石墨电极.接通电源,经过一段时间后,测得乙中c电极质量增加了16g.常温下各烧杯中溶液的pH与电解时间t的关系如图2.据此回答下列问题:
(1)电极b上发生的电极反应为4OH--4e-=2H2O+O2↑.
(2)写出乙烧杯的电解池总反应化学方程式2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4.
(3)用惰性电极电解B溶液,当阳离子浓度下降至一半时停止通电,加入下列物质不能使该溶液恢复至起始状态的是C.
A、CuO B、CuO C、Cu(OH)2 D、CuCO3
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行能(填“能”或“不能”).
(5)计算电极e上生成的气体在标准状态下的体积5.6L.
(6)要使丙烧杯溶液恢复到原来的状态,操作是向丙烧杯中加入4.5g水.
| 阳离子 | Na+、K+、Cu2+ |
| 阴离子 | SO${\;}_{4}^{2-}$、OH- |

(1)电极b上发生的电极反应为4OH--4e-=2H2O+O2↑.
(2)写出乙烧杯的电解池总反应化学方程式2CuSO4+2H2O$\frac{\underline{\;通电\;}}{\;}$2Cu+O2↑+2H2SO4.
(3)用惰性电极电解B溶液,当阳离子浓度下降至一半时停止通电,加入下列物质不能使该溶液恢复至起始状态的是C.
A、CuO B、CuO C、Cu(OH)2 D、CuCO3
(4)如果电解过程中B溶液中的金属离子全部析出,此时电解能否继续进行能(填“能”或“不能”).
(5)计算电极e上生成的气体在标准状态下的体积5.6L.
(6)要使丙烧杯溶液恢复到原来的状态,操作是向丙烧杯中加入4.5g水.
3.在下列条件下,一定能大量共存的微粒组是( )
| A. | 甲基橙呈黄色的溶液中:K+、Na+、SO42-、S2O32- | |
| B. | 能与Al反应生成H2的溶液:Na+、Ba2+、NO3-、I- | |
| C. | 常温下水电离出的OH-为1×10-7mol/L的溶液中:K+、Na+、SO42-、AlO2- | |
| D. | 常温下pH=7的溶液中:NH4+、K+、CH3COO-、NO3- |
10.下列各项操作中,发生“先产生沉淀,后沉淀又溶解”现象的是( )
①向AlCl3溶液中通入过量的NH3 ②向Fe(OH)3胶体中逐滴加入过量的稀硫酸
③向NaAlO2溶液中逐滴加入过量的盐酸 ④向Ca(OH)2溶液中逐渐通入过量的CO2.
①向AlCl3溶液中通入过量的NH3 ②向Fe(OH)3胶体中逐滴加入过量的稀硫酸
③向NaAlO2溶液中逐滴加入过量的盐酸 ④向Ca(OH)2溶液中逐渐通入过量的CO2.
| A. | ①②④ | B. | ①③④ | C. | ②③④ | D. | ①②③ |
20.下列离子在溶液中能大量共存的是( )
| A. | Cl-、NO3-、Fe3+、Na+ | B. | Ag+、NO3-、Cl-、K+ | ||
| C. | K+、Ba2+、OH-、SO42- | D. | Cu2+、NH4+、Br-、OH- |
7.下列与实验相关的叙述正确的是( )
| A. | 稀释浓硫酸时,应将蒸馏水沿玻璃棒缓慢注入浓硫酸中 | |
| B. | 用浓硫酸配制一定物质的量浓度的硫酸溶液时,溶解后的溶液未冷却至室温就转移入容量瓶,会造成所配溶液浓度偏高 | |
| C. | 溶液加入稀盐酸产生无色气体,将气体通入澄清石灰水,变浑浊,原溶液一定含有CO32- | |
| D. | 检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
4.成语是中华民族灿烂文化中的瑰宝,下列涉及氧化还原反应的是( )
| A. | 蜡炬成灰 | B. | 木已成舟 | C. | 铁柱成针 | D. | 滴水成冰 |
5.X、Y、Z、W是分别位于第2、3周期的元素,原子序数依次递增.X与Z位于同一主族,Y元素的单质既能与盐酸反应也能与NaOH溶液反应,Z原子的最外层电子数是次外层电子数的一半,Y、Z、W原子的最外层电子数之和为14.下列说法正确的是( )
| A. | 原子半径由小到大的顺序:X<Y<Z<W | |
| B. | X氢化物的沸点高于Z氢化物的沸点 | |
| C. | 最高价氧化物对应水化物的酸性X大于Z | |
| D. | 室温下,0.1 mol/L W的气态氢化物的水溶液的pH>1 |