题目内容
11.25℃时,下列有关0.10mol/L Na2SO3溶液(忽略溶液体积变化及被空气氧化)的叙述正确的是( )| A. | 与漂白粉溶液反应的离子方程式:Ca2++SO32-=CaSO3↓ | |
| B. | 通入HCl至溶液pH=7:c(Na+)=2c(SO32-)+c(HSO3-)+c(Cl-) | |
| C. | 加入NaOH固体可使溶液中水的电离程度增大 | |
| D. | 通入SO2至过量:c(Na+)=2[c(SO32-)+c(HSO3-)+c(H2SO3)] |
分析 A.漂白粉具有强氧化性,能够将亚硫酸钙氧化成硫酸根;
B.反应后为中性时,根据电荷守恒判断;
C.加入氢氧化钠溶液,氢氧根离子抑制了水的电离;
D.二氧化硫过量,反应生成亚硫酸氢钙,根据亚硫酸氢钙溶液中的物料守恒分析.
解答 解:A.亚硫酸钙被次氯酸根离子氧化成硫酸钙,正确的离子方程式为:Ca2++ClO-+SO32-═CaSO4↓+Cl-,故A错误;
B.通入HCl至溶液pH=7,根据电荷守恒有:c(Na+)+c(H+)=2c(SO32-)+c(HSO3-)+c(OH-)+c(Cl-),其中c(H+)=c(OH-),故B正确;
C.氢氧化钠溶液中的氢氧根离子抑制了水的电离,则加入氢氧化钠后水的电离程度减小,故C错误;
D.通入SO2至过量,反应后溶质为亚硫酸氢钙,根据物料守恒可得:c(Na+)=c(SO32-)+c(HSO3-)+c(H2SO3),故D错误;
故选:B.
点评 本题考查了离子浓度大小比较,题目难度中等,明确盐的水解原理、氧化还原反应实质为解答关键,注意掌握电荷守恒、物料守恒的含义及应用方法,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
1.下列颜色变化与氧化还原反应无关的是( )
| A. | 长期放置的苯酚晶体变红 | B. | 硝酸银晶体光照后变黑 | ||
| C. | 氢氧化亚铁变灰绿再变红褐 | D. | 二氧化碳气体冷却后变淡 |
6. 碳及其化合物在科技、社会生产、生活中有着广泛的应用.请按要求回答下列问题:
碳及其化合物在科技、社会生产、生活中有着广泛的应用.请按要求回答下列问题:
(1)已知:2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H1=-1214.6kJ/mol
2CO(g)+O2(g)═2CO2(g)△H2=-566kJ/mol
请写出CH4燃烧热的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
(2)在不同温度下反应CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常数K如下表:
①该反应的△H<0.(填“>”、“=”或“<”).
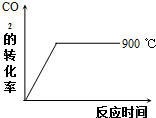
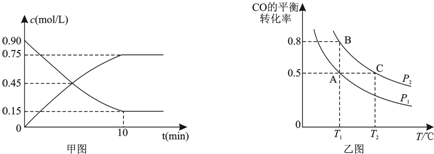
②900℃时发生上述反应,CO2的转化率随时间变化如图所示,若到达平衡后加压,则H2的转化率将(填“增大”、“减小”或“不变”,下同)不变,正反应速率将增大.
其他条件相同时,请在图中画出750℃时CO2的转化率随时间变化的示意图.
③在900℃时发生上述反应,以下表中的物质的量投入恒容反应器,其中向正方向移动的组是(填编号)AD,平衡后与C中各物质的百分含量相等的组有BD(填编号)
(3)以二甲醚(CH3OCH3)、空气、KOH溶液为原料可设计为燃料电池
①放电时,负极电极反应式:CH3OCH3-12e-+16OH-=2CO32-+11H2O.
②假设该燃料电池中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为6.72L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
 碳及其化合物在科技、社会生产、生活中有着广泛的应用.请按要求回答下列问题:
碳及其化合物在科技、社会生产、生活中有着广泛的应用.请按要求回答下列问题:(1)已知:2CH4(g)+3O2(g)═2CO(g)+4H2O(l)△H1=-1214.6kJ/mol
2CO(g)+O2(g)═2CO2(g)△H2=-566kJ/mol
请写出CH4燃烧热的热化学方程式:CH4(g)+2O2(g)=CO2(g)+2H2O(l)△H=-890.3kJ/mol.
(2)在不同温度下反应CO2(g)+H2(g)?CO(g)+H2O(g)的平衡常数K如下表:
| 温度/℃ | 600 | 750 | 900 | 1100 | 1250 |
| 平衡常数K | 2.5 | 1.6 | 1 | 0.9 | 0.6 |
②900℃时发生上述反应,CO2的转化率随时间变化如图所示,若到达平衡后加压,则H2的转化率将(填“增大”、“减小”或“不变”,下同)不变,正反应速率将增大.
其他条件相同时,请在图中画出750℃时CO2的转化率随时间变化的示意图.
③在900℃时发生上述反应,以下表中的物质的量投入恒容反应器,其中向正方向移动的组是(填编号)AD,平衡后与C中各物质的百分含量相等的组有BD(填编号)
| A | B | C | D | E | |
| n(CO2) | 3 | 1 | 0 | 1 | 1 |
| n(H2) | 2 | 1 | 0 | 1 | 2 |
| n(CO) | 1 | 2 | 3 | 0.5 | 3 |
| n(H2O) | 5 | 2 | 3 | 0.5 | 1 |
①放电时,负极电极反应式:CH3OCH3-12e-+16OH-=2CO32-+11H2O.
②假设该燃料电池中盛有100.0mL 3.0mol/L KOH溶液,放电时参与反应的氧气在标准状况下的体积为6.72L,放电过程中没有气体逸出,则放电完毕后,所得溶液中各离子浓度由大到小的关系为c(K+)>c(CO32-)>c(OH-)>c(HCO3-)>c(H+).
20.下列说法正确的是( )
| A. | 25℃时,将pH=a的一元强酸溶液与pH=14-a的一元碱溶液等体积混合后,所得溶液呈酸性或中性 | |
| B. | 相同温度的盐酸和醋酸两种溶液中,若c(Cl-)=c(CH3COO-),则两溶液pH相同 | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合所得溶液中:c(CO32-)+2c(OH-)═c(HCO3-)+c(H2CO3)+2c(H+) | |
| D. | 对于沉淀溶解平衡AgX?Ag++X-,已知AgCl的平衡常数大于AgI.则含AgCl和AgI固体的悬浊液中存在:c(Ag+)>c(I-)>c(Cl-) |
8.某学生用0.2000mol•L-1的标准NaOH溶液滴定未知浓度的盐酸,其操作步骤如下:
①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液.
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
请回答下列问题:
(1)步骤①中,量取20.00mL待测液应使用酸式滴定管(填仪器名称),若在锥形瓶装液前残留少量蒸馏水,将使测定结果无影响(填“偏大”、“偏小”或“无影响”).
(2)步骤②中,滴定时眼睛应注视锥形瓶(填仪器名称),判断到达滴定终点的依据是滴入最后一滴NaOH溶液,锥形瓶中溶液由无色变为浅红色,半分钟不变色.
(3)第一次滴定记录的NaOH溶液的体积明显多于后两次的体积,其可能的原因是AB(填字母)
A.滴定前滴定管尖嘴有气泡,滴定结束时无气泡
B.锥形瓶装液前用待测液润洗
C.NaOH标准液保存时间过长,有部分Na2CO3生成
D.滴定终点时,俯视读数
(4)根据上表记录数据,通过计算可得该盐酸的浓度为0.1626 mol•L-1.
①量取20.00mL待测液注入洁净的锥形瓶中,并加入3滴酚酞溶液.
②用标准液滴定至终点,记录滴定管液面读数,所得数据如下表:
| 滴定次数 | 盐酸体积 | NaOH溶液体积读数(mL) | |
| 滴定前 | 滴定后 | ||
| 1 | 20.00 | 0.00 | 18.10 |
| 2 | 20.00 | 0.00 | 16.30 |
| 3 | 20.00 | 0.00 | 16.22 |
(1)步骤①中,量取20.00mL待测液应使用酸式滴定管(填仪器名称),若在锥形瓶装液前残留少量蒸馏水,将使测定结果无影响(填“偏大”、“偏小”或“无影响”).
(2)步骤②中,滴定时眼睛应注视锥形瓶(填仪器名称),判断到达滴定终点的依据是滴入最后一滴NaOH溶液,锥形瓶中溶液由无色变为浅红色,半分钟不变色.
(3)第一次滴定记录的NaOH溶液的体积明显多于后两次的体积,其可能的原因是AB(填字母)
A.滴定前滴定管尖嘴有气泡,滴定结束时无气泡
B.锥形瓶装液前用待测液润洗
C.NaOH标准液保存时间过长,有部分Na2CO3生成
D.滴定终点时,俯视读数
(4)根据上表记录数据,通过计算可得该盐酸的浓度为0.1626 mol•L-1.
 .
.
 .
.

 +
+ $\stackrel{催化剂}{→}$
$\stackrel{催化剂}{→}$
 .
. .
.