题目内容
15. (1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式,并用双线桥画出电子转移的方向和数目.
(1)瑞典化学家舍勒将软锰矿(主要成分MnO2)与浓盐酸混合加热,在世界上首先制得了氯气.写出该反应的离子方程式,并用双线桥画出电子转移的方向和数目.
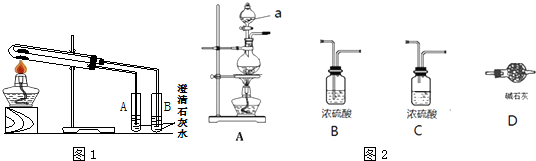
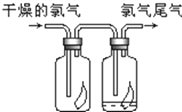
(2)如图所示,将干燥的氯气依次通过盛有干燥的有色布条的广口瓶A和盛有潮湿的有色布条的广口瓶B,可观察到的现象是干燥的有色布条无明显现象,潮湿的有色布条褪色.
(3)工业将氯气通入冷的消石灰中制取漂白粉,其反应的化学方程式为2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O,漂白粉的有效成分是Ca(ClO)2(写化学式),该反应中氧化剂与还原剂物质的量之比是1:1.
(4)①氯气是一种重要的工业原料.工业上利用下列反应:□Cl2+□NH3=□N2+□NH4Cl (配平该方程式,将系数填入□中)
②检查氯气管道是否漏气.请判断下列叙述中正确的是:ABD(写序号)
A.若管道漏气遇氨就会产生白烟 B.该反应利用了氯气的强氧化性
C.该反应属于复分解反应 D.该反应属于置换反应.
分析 (1)实验室用浓盐酸和二氧化锰制取氯气,二者反应生成氯化锰、氯气和水,锰元素化合价+4价降低为+2价,氯元素化合价-1价变化为0价,结合电子守恒标注;
(2)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性;
(3)氯气和消石灰反应生成氯化钙、次氯酸钙和水;漂白粉有效成分为次氯酸钙,该反应中氧化剂与还原剂都是氯气,化合价0甲变化为-1价做氧化剂,化合价变化为+1价做还原剂;
(4)①氯气和氨气发生氧化还原反应生成氮气和氯化铵,氯元素化合价0价变化为-1价,氮元素化合价-3价变化为0价,结合电子守恒和原子守恒配平书写得到化学方程式
②3Cl2+8NH3=N2+6NH4Cl,反应中有化合价变化,属于氧化还原反应,氯元素化合价降低,表现氧化性,生成的氯化氢与氨气极易反应生成氯化铵,氯化铵常温下为白色固体,结合复分解、置换反应的定义解答.
解答 解:(1)Mn元素的化合价由+4价降低为+2价,Cl元素的化合价由-1价升高为0,该反应中转移2e-,用双线桥表示该反应电子转移方向和总数为: ,
,
故答案为: ;
;
(2)氯气无漂白性,氯气与水反应生成的次氯酸具有漂白性,干燥的有色布条无明显现象,潮湿的有色布条褪色;
故答案为:干燥的有色布条无明显现象,潮湿的有色布条褪色;
(3)氯气和氢氧化钙反应生成氯化钙、次氯酸钙、水;其化学方程式为:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O;漂白粉的有效成分是:Ca(ClO)2 ,该反应中氧化剂与还原剂都是氯气,化合价0甲变化为-1价做氧化剂,化合价变化为+1价做还原剂,则氧化剂和还原剂物质的量之比是1:1,
故答案为:2Cl2 +2Ca(OH)2=CaCl2 +Ca(ClO)2 +2H2O;Ca(ClO)2;1:1;
(4)①工业上利用反应氯气和氨气反应生成氮气和氯化铵检查氯气管道是否漏气,氯元素化合价0价变化为-1价,氮元素化合价-3价变化为0价,结合电子守恒和原子守恒配平书写得到化学方程式为:3Cl2+8NH3=N2+6NH4Cl,
②A.反应生成氯化铵,观察到白烟可知管道漏气,故A正确;
B.反应中有化合价变化,属于氧化还原反应,氯元素化合价降低,表现氧化性,故B正确;
C.反应中有单质参加和生成,不属于复分解反应,故C错误;
D.反应符合一种单质和一种化合物反应生成另一种单质和另一种化合物的特点,为置换反应,故D正确;
故选ABD,
故答案为:3,8,1,6;ABD.
点评 本题考查了氯气的制备和性质、氧化还原反应电子转移和配平,明确氯气制备原理及氯气和次氯酸性质的区别是解题关键,注意漂白粉的主要成分与有效成分的区别,注意漂白粉漂白的原理,题目难度中等.

 智趣暑假温故知新系列答案
智趣暑假温故知新系列答案 英语小英雄天天默写系列答案
英语小英雄天天默写系列答案| 软锰矿 | 闪锌矿 |
| MnO2约70%,SiO2约20%,Al2O3约4%,其余为水分 | ZnS约80%,FeS、CuS、SiO2共约7%,其余为水分 |
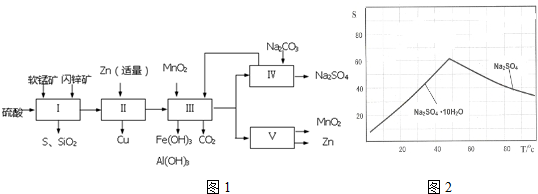
(1)流程Ⅰ所得滤液中含有MnSO4、ZnSO4、CuSO4、Fe2(SO4)3、Al2(SO4)3等,则流程Ⅰ中被氧化的物质有FeS、CuS种.
(2)流程Ⅱ中反应的离子方程式为Zn+Fe3+=Fe2++Zn2+、Zn+Cu2+=Cu+Zn2+.
(3)氢氧化物开始沉淀的pH如表:
| 氢氧化物 | Fe(OH)3 | Al(OH)3 | Fe(OH)2 |
| 开始沉淀pH | 1.5 | 3.3 | 7.6 |
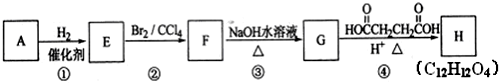
(4)如图2是Na2SO4和Na2SO4•10H2O的溶解度(g/100g水)曲线,又知MnSO4和ZnSO4的溶解度随温度的升高而增大,则流程Ⅳ得到Na2SO4固体的操作是:将分离出MnCO3和ZnCO3后的滤液升温结晶、趁热过滤、乙醇洗涤、干燥,要“趁热”过滤的原因是防止形成Na2SO4•10H2O.
(5)流程Ⅴ的条件是电解,电解时均用惰性电极,阳极发生的电极反应可表示为Mn2+-2e-+2H2O=MnO2+4H+.
(6)取1.95g锌加入到12.00mL 18.4mol/L的浓硫酸中(反应中只生成一种还原产物),充分反应后,小心地将溶液稀释到1000mL,取出15.00mL,以酚酞为指示剂,用0.25mol/L的NaOH溶液滴定余酸,耗用NaOH溶液的体积为21.70mL.
①反应后溶液中多余的硫酸是0.18 mol.
②通过计算确定浓硫酸被还原的产物是S.
| A. | NH4Fe(SO4)2加入过量NaOH溶液中::NH4++Fe3++4OH-═NH3•H2O+Fe(OH)3↓ | |
| B. | 次氯酸钠溶液中通入过量的二氧化硫:ClO-+SO2+H2O═HSO3-+HClO | |
| C. | Ba(OH)2溶液和稀硫酸反应:Ba2++OH-+H++SO42-═BaSO4↓+H2O | |
| D. | 澄清的石灰水中加入过量的NaHCO3溶液:Ca2++OH-+HCO3-═CaCO3↓+H2O |
| A. | 只有① | B. | ①③ | C. | ①②③⑤ | D. | ②③④⑤ |
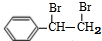
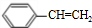 +Br2→
+Br2→