题目内容
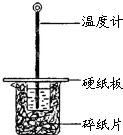 某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法不正确的是( )
某同学用50mL 0.50mol/L的盐酸与50mL 0.55mol/L的NaOH溶液在如图所示的装置中进行中和反应.通过测定反应过程中所放出的热量计算中和热.下列说法不正确的是( )| A、该实验也可在保温杯中进行 |
| B、图中实验装置缺少环形玻璃搅拌棒 |
| C、烧杯间填满碎纸条的作用是保温、隔热,减少热量损失 |
| D、若将盐酸体积改为60 mL,两次实验所求得中和热不相等 |
考点:中和热的测定
专题:化学反应中的能量变化
分析:A、该实验的原理是测反应前后的温度,成败的关键是保温,据此选择反应的仪器即可;
B、根据量热计的构造来判断该装置的缺少仪器;
C、中和热测定实验成败的关键是保温工作,烧杯间填满碎纸条的作用是保温;
D、中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关.
B、根据量热计的构造来判断该装置的缺少仪器;
C、中和热测定实验成败的关键是保温工作,烧杯间填满碎纸条的作用是保温;
D、中和热是强酸和强碱反应生成1mol水时放出的热量,与酸碱的用量无关.
解答:
解:A、该实验的原理是测反应前后的温度,成败的关键是保温,大小烧杯间填充碎纸片或是泡沫,可以用保温杯代替,故A正确;
B、根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,故B正确;
C、中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故C正确;
D、因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关,若将盐酸体积改为60 mL,两次实验所求得中和热相等,故D错误;
故选D.
B、根据量热计的构造可知该装置的缺少仪器是环形玻璃搅拌器,故B正确;
C、中和热测定实验成败的关键是保温工作,大小烧杯之间填满碎纸条的作用是减少实验过程中的热量损失,故C正确;
D、因为中和热是指酸跟碱发生中和反应生成1molH2O所放出的热量,与酸碱的用量无关,若将盐酸体积改为60 mL,两次实验所求得中和热相等,故D错误;
故选D.
点评:本题考查中和热的测定,题目难度不大,注意理解中和热的概念是解题的关键.

练习册系列答案
相关题目
下列有关工业生产的叙述正确的是( )
| A、合成氨生产过程中将NH3液化分离,可加快正反应速率,提高N2?H2的转化率 |
| B、工业上利用电解熔融的氧化铝制取铝,电解熔融的氧化镁制取镁 |
| C、电解精炼铜时,同一时间内阴极溶解铜的质量比阳极析出铜的质量小 |
| D、从海带中提取碘单质的实验中,要经过煅烧、溶解、过滤和萃取等操作 |
温度为T℃时,向2.0L恒容密闭容器中充入1.0mol PCl5,反应PCl5(g)?PCl3(g)+Cl2(g)经一段时间后达到平衡.反应过程中测定的部分数据见下表:下列说法正确的是( )
| t/s | 0 | 50 | 150 | 250 | 350 |
| n(PCl3)/mol | 0 | 0.16 | 0.19 | 0.20 | 0.20 |
| A、反应在前50 s的平均速率为v(PCl3)=0.0032 mol?L-1?s-1 |
| B、T℃时,该反应的平衡常数为0.025 |
| C、保持其他条件不变,升高温度,平衡时c(PCl3)=0.11 mol?L-1,则反应的△H<0 |
| D、相同温度下,向容器中再充入1.0 mol PCl5,达到平衡时,PCl5的转化率大于20% |

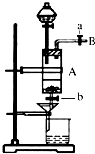 三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl3?6H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,用分液漏斗向A中加过量的盐酸,此时溶液呈浅绿色,再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3?6H2O晶体.
三氯化铁是中学化学实验室中常用的化学试剂.同学们利用废铁屑(含少量铜杂质)来探究制备FeCl3?6H2O的方法,同学甲设计的实验装置如图所示,其实验步骤如下:A中放有废铁屑,烧杯中盛有过量的稀硝酸,实验时打开a,关闭b,用分液漏斗向A中加过量的盐酸,此时溶液呈浅绿色,再打开b进行过滤,过滤结束后,取烧杯内溶液倒入蒸发皿加热,蒸发掉部分水并使剩余HNO3分解,再降温结晶得FeCl3?6H2O晶体. 人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度:
人体血液里Ca2+离子的浓度一般采用g/cm3来表示.抽取一定体积的血样,加适量的草酸铵[(NH4)2C2O4]溶液,可析出草酸钙(CaC2O4)沉淀,将此草酸钙沉淀洗涤后溶于强酸可得草酸(H2C2O4),再用KMnO4溶液滴定即可测定血液样品中Ca2+的浓度.某研究性学习小组设计如下实验步骤测定血液样品中Ca2+的浓度: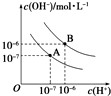 已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示:
已知水在25℃(A)和T℃(B)时,其电离平衡曲线如图所示: