题目内容
7.为了减少煤燃烧对大气造成的污染,煤的气化和液化是高效、清洁利用煤炭的重要途径,而减少CO2气体的排放也是人类面临的重大课题.煤综合利用的一种途径如图1所示: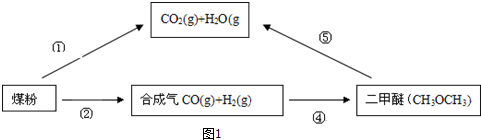
(1)用图2所示装置定量检测过程①产生的CO2(已知:煤粉燃烧过程中会产生SO2)
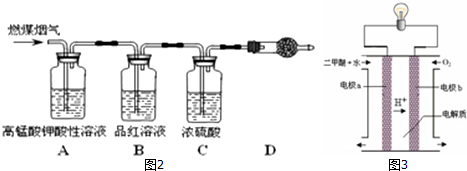
B中预期的实验现象是品红溶液不变色,D中的试剂是碱石灰.
(2)已知C(s)+H2O(g)═CO(g)+H2(g)△H1=+131.3kJ•mol-1
C(s)+2H2O(g)═CO2(g)+2H2(g)△H2=+90kJ•mol-1
则一氧化碳与水蒸气反应生成二氧化碳和氢气的热化学方程式是CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.3kJ•mol-1.
(3)用图3装置可以完成⑤的转化,同时提高能量的利用率.其实现的能量转化形式主要是化学能转变成电能,a的电极反应式是CH3OCH3-12e-+3H2O=2CO2↑+12H+.
(4)燃煤烟气中的CO2可用稀氨水捕获和吸收,不仅可以减少CO2的排放,也可以生产化肥碳酸氢铵.假设该方法每小时处理含CO2的体积分数为11.2%的燃煤烟气1000m3(标准状况),其中CO2的脱除效率为80%,则理论上每小时生产碳酸氢铵316kg.
分析 (1)根据燃煤烟气的成分为:CO2、SO2、CO、H2O,酸性高锰酸钾能够除去SO2,CO2、CO、H2O不能使品红溶液褪色,浓硫酸可以吸水;根据碱石灰能够吸收CO2;
(2)根据盖斯定律来解答;
(3)根据原电池将化学能转变成电能;根据负极的电极反应=总反应-正极的电极反应;
(4)根据方程式CO2+NH3•H2O=NH4HCO3来计算.
解答 解:(1)燃煤烟气的成分为:CO2、SO2、CO、H2O,酸性高锰酸钾能够除去SO2,CO2、CO、H2O不能使品红溶液褪色,碱石灰能够吸收CO2;
故答案为:品红溶液不变色;碱石灰;
(2)C(s)+H2O(g)=CO(g)+H2(g)△H1=+131.3kJ•mol-1 ①
C(s)+2H2O(g)=CO2(g)+2H2(g)△H2=+90kJ•mol-1 ②
由盖斯定律②-①得:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.3kJ•mol-1
故答案为:CO(g)+H2O(g)=CO2(g)+H2(g)△H=-41.3kJ•mol-1;
(3)图3装置是原电池,将化学能转变成电能;正极上是氧气发生得电子的还原反应:3O2+12e-+12H+=6H2O,总反应:CH3OCH3+3O2=2CO2+3H2O,负极的电极反应:CH3OCH3+3H2O-12e-=2CO2↑+12H+,
故答案为:化学能转变成电能;CH3OCH3-12e-+3H2O=2CO2↑+12H+;
(4)CO2 +NH3•H2O=NH4HCO3
1 1
$\frac{1000×1{0}^{3}L×11.2%×80%}{22.4L/mol}$ 4000mol
所以NH4HCO3 的质量m=4000mol×79g/mol=316000g=316kg;
故答案为:316.
点评 本题考查的知识点较多,综合性较强,涉及盖斯定律的应用、电极方程式、物质的性质以及化学计算,注意知识的归纳和整理是关键,题目难度中等.

 一线名师提优试卷系列答案
一线名师提优试卷系列答案 阳光试卷单元测试卷系列答案
阳光试卷单元测试卷系列答案| A. | 二氧化碳与超临界水作用生成汽油的反应,属于放热反应 | |
| B. | “水热反应”是一种复杂的物理化学变化 | |
| C. | 火力发电厂可以利用废热,将二氧化碳转变为能源物质 | |
| D. | 随着科技的进步,“水热反应”制取能源有望实现地球上碳资源的和谐循环 |
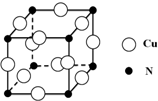
| A. | 由6molCuFeS2生成6molCu,共消耗16.5molO2 | |
| B. | 该冶炼方法中产生大量的有害气体SO2,可回收用于制取硫酸 | |
| C. | 在反应③中,Cu2S既是氧化剂,又是还原剂 | |
| D. | 在反应①中,SO2既是氧化产物,又是还原产物 |
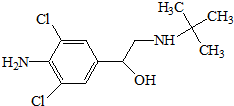 瘦肉精,学名盐酸克伦特罗,该药物既不是兽药,也不是饲料添加剂,而是肾上腺类神经兴奋剂,可以增加动物的瘦肉量.减少饲料使用.使肉品提早上市,降低成本,但对人体会产生副作用,盐酸克伦特罗分子结构简式如图.下列说法不正确的是( )
瘦肉精,学名盐酸克伦特罗,该药物既不是兽药,也不是饲料添加剂,而是肾上腺类神经兴奋剂,可以增加动物的瘦肉量.减少饲料使用.使肉品提早上市,降低成本,但对人体会产生副作用,盐酸克伦特罗分子结构简式如图.下列说法不正确的是( )| A. | 瘦肉精的分子式是C11H18ON2Cl2 | |
| B. | 物质能发生取代反应、氧化反应、加成反应和水解反应 | |
| C. | 1mol盐酸克伦特罗最多能与4molNaOH反应 | |
| D. | 盐酸克伦特罗分子中至少有7个碳原子共面 |
| A. | HCl、HBr、HI的熔、沸点依次升高与分子间作用力大小有关 | |
| B. | H2O的熔、沸点高于H2S是由于H2O分子之间存在氢键 | |
| C. | I2易溶于CCl4可以用相似相溶原理解释 | |
| D. | 甲烷可与水形成氢键这种化学键 |
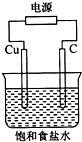
| A. | 石墨电极与直流电源负极相连 | |
| B. | 铜电极的反应式为:2H++2e-═H2↑ | |
| C. | 氢氧化钠在石墨电极附近产生,Na+向石墨电极迁移 | |
| D. | 用湿润KI淀粉试剂在铜电极附近检验气体,试纸变蓝色 |
 硼和氮元素在化学中有很重要的地位,回答下列问题:
硼和氮元素在化学中有很重要的地位,回答下列问题: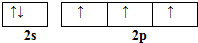 .预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.
.预计于2017年发射的“嫦娥五号”探测器采用的长征5号运载火箭燃料为偏二甲肼[(CH3)2NNH2].(CH3)2NNH2中N原子的杂化方式为sp3.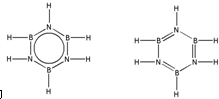 .
.
