题目内容
13.下列有关离子键和离子化合物的说法正确的是( )| A. | 凡含离子键的化合物,一定含金属元素 | |
| B. | 在化合物MgCl2中,两个氯离子之间也存在离子键 | |
| C. | 离子化合物中不可能有共价键 | |
| D. | 原子序数为11与9的元素能够形成离子化合物,该化合物中存在离子键 |
分析 A.离子化合物中一定含有离子键,但不一定含有金属元素;
B.氯化镁中只存在镁离子和氯离子之间的化学键;
C.离子化合物中一定含有离子键,可能含有共价键;
D.活泼金属和活泼非金属元素之间易形成离子键.
解答 解:A.离子化合物中一定含有离子键,但不一定含有金属元素,如铵盐,故A错误;
B.氯化镁中只存在镁离子和氯离子之间的化学键,两个氯离子之间不存在化学键,故B错误;
C.离子化合物中一定含有离子键,可能含有共价键,如KOH等,故C错误;
D.活泼金属和活泼非金属元素之间易形成离子键,11号元素是Na元素、9号元素是F元素,二者通过得失电子形成离子键,如D正确;
故选D.
点评 本题考查化学键,为高频考点,明确物质构成微粒及微粒之间作用力是解本题关键,采用举例法分析解答,易错选项是AB.

练习册系列答案
相关题目
4.将铁屑溶于过量的稀盐酸后,再加入下列物质,溶液中铁元素只以Fe2+存在的是( )
| A. | 氯水 | B. | 稀硫酸 | C. | KMnO4溶液 | D. | 双氧水 |
1.在下面的电子结构中,第一电离能最小的原子可能是( )
| A. | 3s23p3 | B. | 3s23p5 | C. | 3s23p4 | D. | 3s23p6 |
8.下列物质的电子式书写正确的是( )
| A. | 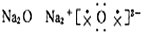 | B. | 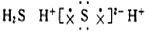 | C. | 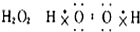 | D. | N2 N:::N |
18.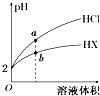 25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
 25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )
25℃时,将pH均为2的HCl与HX的溶液分别加水稀释,溶液pH随溶液体积变化的曲线如图所示.下列说法正确的是( )| A. | a、b两点:c(X-)>c(Cl-) | B. | 稀释10倍,HX溶液的pH=3 | ||
| C. | 稀释前,c(HX)=0.01 mol•L-1 | D. | 溶液的导电性:a>b |
5.X、Y、Z、W均为短周期元素,它们在元素周期表中的位置如下表所示.若Y原子的最外层电子数是次外层电子数的3倍,下列说法中正确的是( )
| X | Y | |
| Z | W |
| A. | 原子半径:W>Z>Y>X | |
| B. | 最高价氧化物对应水化物的酸性:Z>W>X | |
| C. | 四种元素的单质中,Z单质的熔沸点最高 | |
| D. | X的单质能与H2反应,生成一种弱酸性的物质 |
2.下表列出前20号元素中的某些元素性质的一些数据:
试回答下列问题:
(1)以上10种元素中,第一电离能最小的是②(填编号);
(2)元素⑨和⑩形成的化合物的化学式为Si3N4;元素⑦的原子价电子排布式是3s23p5;
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°.三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键--三个原子均等地享有这四个电子,这种特殊的共价键的类型是π键(填σ或π),在高中化学中有一种常见分子的结合方式与O3相同,它是SO2(填分子式);
(4)根据对角线规则,Be与元素④的最高价氧化物的水化物的性质相似,它们都具有两性,显示这种性质的离子方程式是Be(OH)2+2H+═Be2++2H2O、Be(OH)2+2OH-═BeO22-+2H2O;
(5)由以上某些元素形成的有机物苯酚(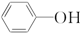 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子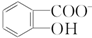 能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是
能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是 中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
| 元素 性质 | ① | ② | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ | ⑩ |
| 原子半径 (10-10m) | 1.02 | 2.27 | 0.74 | 1.43 | 0.77 | 1.10 | 0.99 | 1.86 | 0.75 | 1.17 |
| 最高价态 | +6 | +1 | - | +3 | +4 | +5 | +7 | +1 | +5 | +4 |
| 最低价态 | -2 | - | -2 | - | -4 | -3 | -1 | - | -3 | -4 |
(1)以上10种元素中,第一电离能最小的是②(填编号);
(2)元素⑨和⑩形成的化合物的化学式为Si3N4;元素⑦的原子价电子排布式是3s23p5;
(3)元素③有一种单质为O3,其分子呈V形结构,键角116.5°.三个原子以一个为中心,与另外两个原子分别构成一个非极性键,中心原子再提供2个电子,旁边两原子各提供一个电子构成一个特殊的共价键--三个原子均等地享有这四个电子,这种特殊的共价键的类型是π键(填σ或π),在高中化学中有一种常见分子的结合方式与O3相同,它是SO2(填分子式);
(4)根据对角线规则,Be与元素④的最高价氧化物的水化物的性质相似,它们都具有两性,显示这种性质的离子方程式是Be(OH)2+2H+═Be2++2H2O、Be(OH)2+2OH-═BeO22-+2H2O;
(5)由以上某些元素形成的有机物苯酚(
 )具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子
)具有弱酸性,其Ka=1.1×10-10;水杨酸第一级电离形成的离子 能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是
能形成分子内氢键.据此判断,相同温度下电离平衡常数Ka2(水杨酸)<Ka(苯酚)(填“>”或“<”),其原因是 中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
中形成分子内氢键,使其更难电离出H+;水杨酸分子中苯环和羧基上碳原子的杂化方式分别是sp2杂化和sp2杂化.
3.基态原子的4s能级中只有1个电子的元素共有( )
| A. | 1 种 | B. | 2 种 | C. | 3 种 | D. | 8 种 |
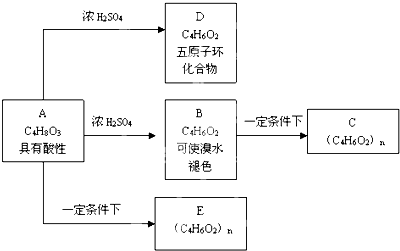
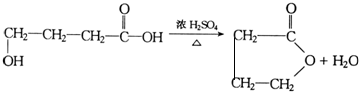

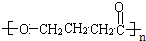 +nH2O
+nH2O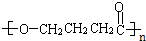 ;
;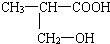 及
及 .
.