题目内容
 CH3COOH为常见的弱酸,在工业生产和生活中有广泛的应用.
CH3COOH为常见的弱酸,在工业生产和生活中有广泛的应用.(1)常温下中和100mL pH=3的CH3COOH溶液和1L pH=4的CH3COOH溶液,需要等物质的量浓度的NaOH溶液的体积分别为V1和V2,则V1
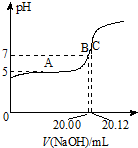
(2)常温下,用0.1000mol/L的NaOH溶液滴定20.00mL某未知浓度的CH3COOH溶液,滴定曲线如图所示.其中A点所示溶液中c(CH3COO-)=2c(CH3COOH),C点所示溶液中存在c(CH3COO-)+c(CH3COOH)=c(Na+).则常温下CH3COOH的电离常数Ka=
考点:酸碱混合时的定性判断及有关ph的计算
专题:电离平衡与溶液的pH专题
分析:(1)相同温度下,酸的浓度越小其电离程度越大,醋酸和碱反应消耗碱的物质的量与酸的物质的量成正比;
(2)根据C中物料守恒计算醋酸浓度,再根据pH=pKa-lgc(CH3COO-)/lgc(CH3COOH)计算电离平衡常数.
(2)根据C中物料守恒计算醋酸浓度,再根据pH=pKa-lgc(CH3COO-)/lgc(CH3COOH)计算电离平衡常数.
解答:
解:(1)相同温度下,酸的浓度越小其电离程度越大,所以pH=3醋酸的浓度大于pH=4醋酸浓度的10倍,100mL pH=3的CH3COOH溶液和1L pH=4的CH3COOH溶液,前者的物质的量大于后者,醋酸和碱反应消耗碱的物质的量与酸的物质的量成正比,所以消耗氢氧化钠体积V1>V2,故答案为:>;
(2)根据C中物料守恒得醋酸浓度=
=0.1006mol/L,A为缓冲溶液,pH=pKa-lgc(CH3COO-)/lgc(CH3COOH),5=pKa-lg2,10-5=
,Ka=2×10-5,故答案为:2×10-5;0.1006 mol/L.
(2)根据C中物料守恒得醋酸浓度=
| 0.02012L×0.1L/mol |
| 0.020L |
| Ka |
| 2 |
点评:本题考查了弱电解质的电离,根据弱电解质的电离平衡特点、酸碱混合溶液酸碱性等知识点来分析解答,灵活运用微粒间关系找出这几个常数之间的关系式,同时考查学生灵活运用知识能力,题目难度较大.

练习册系列答案
相关题目
用特殊的方法把固体物质加工到纳米级的超细粉末粒子,然后制得纳米材料.下列分散系中分散质的微粒直径和这种粒子具有相同数量级的是( )
| A、溶液 | B、悬浊液 |
| C、胶体 | D、乳浊液 |
某原子的基态电子排布为1s22s22p63s23p63d64s2,该元素不可能的价态是( )
| A、-1 | B、+2 | C、+3 | D、0 |
设NA为阿伏加德罗常数的数值,下列说法正确的是( )
| A、铁与足量稀硝酸反应,1 mol Fe失去电子数为3NA |
| B、常温常压下,22.4L 乙烯中含极性共价键数目为5NA |
| C、1 mol Cu与足量浓硫酸反应产生2NA个SO2分子 |
| D、1 mol冰醋酸和1 mol乙醇在浓硫酸加热下充分反应生成H2O个数为NA |
某强碱性溶液中含有的离子是K+、NH4+、A13+、AlO2-、CO32-、SiO32-、Cl-中的某几种,现进行如下实验:
①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
③另取一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.2153g.
下列说法中正确的是( )
①取少量的溶液用硝酸酸化后,该溶液无沉淀生成;
②另取一定量原溶液,逐滴加入盐酸至过量,发生的现象是:开始产生沉淀并逐渐增多,沉淀量基本不变后产生一种气体,最后沉淀逐渐减少至消失.
③另取一定量的原溶液中加入5mL0.2mol/L盐酸时,沉淀会完全消失,加入足量的硝酸银溶液可得到沉淀0.2153g.
下列说法中正确的是( )
| A、该溶液中一定不含NH4+、A13+、SiO32-、Cl- |
| B、该溶液中一定含有A13+、CO32-、Cl- |
| C、该溶液中一定含有K+、AlO2-、CO32-、Cl- |
| D、Cl-可能含有 |
下列实验方案合理的是( )

| A、配制银氨溶液:质量分数为2% 氨水中加入过量的硝酸银溶液 |
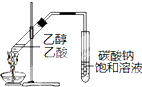
| B、制备乙酸乙酯:用如右图所示的实验装置 |
| C、鉴定溴乙烷中的溴原子:向溴乙烷中加入硝酸酸化的硝酸银溶液 |
| D、鉴别地沟油和矿物油:加入足量氢氧化钠溶液加热 |
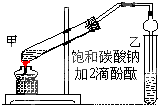 实验室制取乙酸乙酯的主要步骤如下:
实验室制取乙酸乙酯的主要步骤如下: