题目内容
3.下列说法正确的是( )| A. | 推广使用煤的液化技术,从根本上减少二氧化碳等温室效应的排放 | |
| B. | 胶体和溶液的本质区别是胶体具有丁达尔现象 | |
| C. | SiO2既能与氢氧化钠溶液反应又能与氢氟酸反应,SiO2是两性氧化物 | |
| D. | 使用含有氯化钙的融雪剂会加速桥梁的腐蚀 |
分析 A、煤经液化能变为甲醇;
B、胶体本质特征为分散质粒度介于1-100nm;
C、SiO2既能与氢氧化钠溶液反应又能与氢氟酸反应,但是二氧化硅不能与学生、硫酸等强酸反应,不属于两性氧化物;
D、原电池能加快化学反应的速率.
解答 解:A、煤经液化能变为甲醇,燃烧仍生成二氧化碳,故不能减少二氧化碳的排放,故A错误;
B、胶体和溶液的本质区别是分散质粒度大小不同,所以可以用丁达尔现象来区分,故B错误;
C、SiO2为酸性氧化物,能与氢氧化钠溶液反应,不能与强酸反应,与氢氟酸反应是由于氟化氢具有腐蚀性,所以SiO2不是两性氧化物,故C错误;
D、氯化钙是电解质,能与桥梁中的钢构成原电池,故D正确;
故选D.
点评 本题考查了物质的用途,熟悉过二氧化硅、胶体的性质,明确金属电化学腐蚀原理是解题关键,题目难度不大.

练习册系列答案
 课堂练加测系列答案
课堂练加测系列答案 轻松课堂单元测试AB卷系列答案
轻松课堂单元测试AB卷系列答案
相关题目
14.用H2可将工业废气中的NO催化还原成N2,其它量的转化关系如图所示(图中计量单位为mol),则:
NO(g)+H2(g)=$\frac{1}{2}$N2(g)+H2O(g)的△H为( )
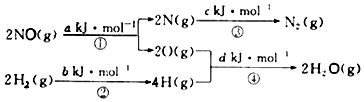
NO(g)+H2(g)=$\frac{1}{2}$N2(g)+H2O(g)的△H为( )

| A. | 0.5(a+b-c-d)kJ/mol | B. | 0.5(c+a-d-b)kJ/mol | ||
| C. | 0.5(c+d-a-b)kJ/mol | D. | 0.5(c+d-a-b)kJ/mol |
8. 铁是生产生活中应用最广泛的金属,炼铁技术备受关注,已知:
铁是生产生活中应用最广泛的金属,炼铁技术备受关注,已知:
①2Fe2O3(s)+3C(s)?4Fe(s)+3CO2(g)△H=+460.5kJ•mol-1
②Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJ•mol-1
③断裂1mol CO(s)气体中的化学键需要吸收1076kJ的能量
断裂1mol CO2(s)气体中的化学键需要吸收1490kJ的能量
请回答下列问题:
(1)断裂1mol C(s)中所有化学键需要吸收的能量为834.5kJ.
(2)T1℃时,向密闭容器中加入一定量的Fe2O3和C,发生反应①,达到平衡后,CO2的浓度为a mol•L-1;其他条件不变,缩小容器容积,再次达到平衡时,CO2的浓度为b mol•L-1,则a=b.(选填“>”“<”或“=”)
(3)起始温度均为T2℃时,向容积为10L的三个恒容密闭容器中,分别加入一定量的Fe2O3和CO发生反应②,测得相关数据如表所示:
①T2℃时,容器1中反应的平衡常数K1=64.
②容器2中,5min达到平衡,则0~5min内以CO2表示该反应的速率v(CO2)=0.048mol/(L•min).
③对于三个容器中的反应,下列说法正确的是CD(填选项字母).
A.m>2n
B.容器1和容器2中CO的平衡转化率a1<a2.
C.K1=K3
D.平衡时气体压强:P3>P1
(4)T2℃时,向恒压密闭容器中充入0.5mol Fe2O3和1.0mol CO,发生反应②,CO和CO2的物质的量浓度(c)与时间(t)的关系如图所示.
6min时,改变的外界条件为升温,理由为升温,平衡逆向移动,CO浓度增大,CO2浓度减小.
 铁是生产生活中应用最广泛的金属,炼铁技术备受关注,已知:
铁是生产生活中应用最广泛的金属,炼铁技术备受关注,已知:①2Fe2O3(s)+3C(s)?4Fe(s)+3CO2(g)△H=+460.5kJ•mol-1
②Fe2O3(s)+3CO(g)?2Fe(s)+3CO2(g)△H=-28.5kJ•mol-1
③断裂1mol CO(s)气体中的化学键需要吸收1076kJ的能量
断裂1mol CO2(s)气体中的化学键需要吸收1490kJ的能量
请回答下列问题:
(1)断裂1mol C(s)中所有化学键需要吸收的能量为834.5kJ.
(2)T1℃时,向密闭容器中加入一定量的Fe2O3和C,发生反应①,达到平衡后,CO2的浓度为a mol•L-1;其他条件不变,缩小容器容积,再次达到平衡时,CO2的浓度为b mol•L-1,则a=b.(选填“>”“<”或“=”)
(3)起始温度均为T2℃时,向容积为10L的三个恒容密闭容器中,分别加入一定量的Fe2O3和CO发生反应②,测得相关数据如表所示:
| 编号 | 容器 | 起始时物质的量 mol | 平衡时物质的量/mol | 平衡常数(K) | |
| Fe2O3 | CO | Fe | |||
| 1 | 恒温 | 0.5 | 1.5 | 0.8 | K1 |
| 2 | 恒温 | 2 | 3 | m | K2 |
| 3 | 绝热 | 1 | 1.5 | n | K3 |
②容器2中,5min达到平衡,则0~5min内以CO2表示该反应的速率v(CO2)=0.048mol/(L•min).
③对于三个容器中的反应,下列说法正确的是CD(填选项字母).
A.m>2n
B.容器1和容器2中CO的平衡转化率a1<a2.
C.K1=K3
D.平衡时气体压强:P3>P1
(4)T2℃时,向恒压密闭容器中充入0.5mol Fe2O3和1.0mol CO,发生反应②,CO和CO2的物质的量浓度(c)与时间(t)的关系如图所示.
6min时,改变的外界条件为升温,理由为升温,平衡逆向移动,CO浓度增大,CO2浓度减小.
19.下列物质不是胶体的是( )
| A. | 淀粉溶液 | B. | 酒精溶液 | C. | 豆浆溶液 | D. | 鸡蛋清溶液 |
20.对于反应M+N═P,如果温度每升高10℃,反应速率增加为原来的3倍.在10℃时完成反应的10%需要54min,将温度提高到40℃完成反应的10%,需要的时间为( )
| A. | 2 min | B. | 3 min | C. | 6 min | D. | 9 min |
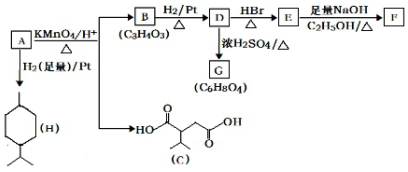
 $→_{△}^{KMnO_{4}/H+}$
$→_{△}^{KMnO_{4}/H+}$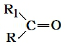 +R2COOH
+R2COOH .
. .
. .
.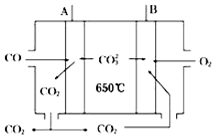 人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.
人们应用原电池原理制作了多种电池,以满足不同的需要.以下每小题中的电池广泛使用于日常生活、生产和科学技术等方面,请根据题中提供的信息,填写空格.