题目内容
某研究性学习小组利用以下装置(部分夹持装置已略,且各装置气密性良好)进行实验探究: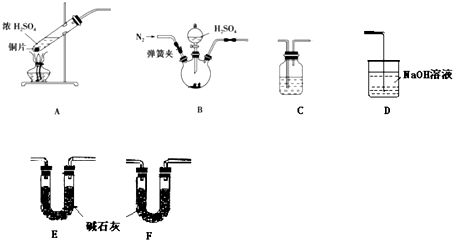
Ⅰ.定性实验:探究SO2能否与BaCl2溶液反应生成BaSO3沉淀.(查阅资料得知常温下BaSO3的Ksp为5.48×10-7,饱和亚硫酸中c(SO32-)=6.3×10-8mol?L-1.浓硫酸的沸点为338℃,酒精灯火焰的温度为400℃~500℃.)
(1)将0.1mol?L-1的BaCl2溶液滴入饱和亚硫酸中, (填“能”或“不能”)生成BaSO3沉淀,原因是 (请通过计算说明原因).
(2)该小组同学用上述装置A、C(盛放BaCl2溶液)、D进行实验,发现C出现白色沉淀,且白色沉淀不溶于盐酸.
①写出A中发生反应的化学方程式: .
②C中BaCl2溶液出现白色沉淀的原因可能是 .
Ⅱ.定量实验:该小组同学欲利用上述部分装置通过测定生成二氧化硫气体的质量,分析某亚硫酸钠样品的纯度(假设杂质与硫酸不反应).
回答下列问题:
(3)按气体流向选用的仪器为: .
(4)若样品质量为m1 g,生成二氧化硫的质量为m2g.该亚硫酸钠样品的纯度 .
(5)为减少实验误差,本实验中很重要的操作是 .

Ⅰ.定性实验:探究SO2能否与BaCl2溶液反应生成BaSO3沉淀.(查阅资料得知常温下BaSO3的Ksp为5.48×10-7,饱和亚硫酸中c(SO32-)=6.3×10-8mol?L-1.浓硫酸的沸点为338℃,酒精灯火焰的温度为400℃~500℃.)
(1)将0.1mol?L-1的BaCl2溶液滴入饱和亚硫酸中,
(2)该小组同学用上述装置A、C(盛放BaCl2溶液)、D进行实验,发现C出现白色沉淀,且白色沉淀不溶于盐酸.
①写出A中发生反应的化学方程式:
②C中BaCl2溶液出现白色沉淀的原因可能是
Ⅱ.定量实验:该小组同学欲利用上述部分装置通过测定生成二氧化硫气体的质量,分析某亚硫酸钠样品的纯度(假设杂质与硫酸不反应).
回答下列问题:
(3)按气体流向选用的仪器为:
(4)若样品质量为m1 g,生成二氧化硫的质量为m2g.该亚硫酸钠样品的纯度
(5)为减少实验误差,本实验中很重要的操作是
考点:探究物质的组成或测量物质的含量,二氧化硫的化学性质
专题:实验探究和数据处理题,氧族元素
分析:(1)若Qc<Ksp,不能生成沉淀;若Qc>Ksp生成沉淀;
(2)由实验装置可知,A中发生Cu与浓硫酸的反应,浓硫酸的沸点为338℃,酒精灯火焰的温度为400℃~500℃,则挥发的部分硫酸与C中硫酸钡反应生成硫酸钡沉淀;
(3)利用上述部分装置通过测定生成二氧化硫气体的质量,B中发生硫酸与亚硫酸的反应,利用氮气将生成的二氧化硫气体赶到C中除杂,然后利用E吸收二氧化硫,最后连接F防止空气中的水、二氧化碳进入E装置,测定E反应前后的质量差可计算亚硫酸钠的质量分数.
(2)由实验装置可知,A中发生Cu与浓硫酸的反应,浓硫酸的沸点为338℃,酒精灯火焰的温度为400℃~500℃,则挥发的部分硫酸与C中硫酸钡反应生成硫酸钡沉淀;
(3)利用上述部分装置通过测定生成二氧化硫气体的质量,B中发生硫酸与亚硫酸的反应,利用氮气将生成的二氧化硫气体赶到C中除杂,然后利用E吸收二氧化硫,最后连接F防止空气中的水、二氧化碳进入E装置,测定E反应前后的质量差可计算亚硫酸钠的质量分数.
解答:
解:(1)0.1mol?L-1的BaCl2溶液滴入饱和亚硫酸中没有沉淀生成,此时溶液中c(Ba2+)<0.1 mol?L-1,c(SO32-)<6.3×10-8mol?L-1,
其浓度商Q=c(Ba2+)×c(SO32-)<0.1×6.3×10-8=6.3×10-9<Ksp(BaSO3)=5.48×10-7;
故答案为:不能;此时溶液中c(Ba2+)<0.1 mol?L-1,c(SO32-)<6.3×10-8mol?L-1,其浓度商Q=c(Ba2+)×c(SO32-)<0.1×6.3×10-8=6.3×10-9<Ksp(BaSO3)=5.48×10-7;
(2)①A中发生Cu与浓硫酸的反应为Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O,故答案为:Cu+2H2SO4(浓)
CuSO4+SO2↑+2H2O;
②C中BaCl2溶液出现白色沉淀的原因为挥发的硫酸与氯化钡反应,故答案为:挥发的硫酸与氯化钡反应;
(3)由实验目的可知,B中发生硫酸与亚硫酸的反应,利用氮气将生成的二氧化硫气体赶到C中除杂,然后利用E吸收二氧化硫,最后连接F防止空气中的水、二氧化碳进入E装置,则按气体流向选用的仪器为BCEF,故答案为:BCEF;
(4)样品质量为m1 g,生成二氧化硫的质量为m2g,亚硫酸钠的质量为
g,该亚硫酸钠样品的纯度为
,故答案为:
;
(5)为减少实验误差,本实验中很重要的操作是反应后要通入氮气一段时间,将装置中生成的二氧化硫全部排入到E装置中,故答案为:反应后要通入氮气一段时间.
其浓度商Q=c(Ba2+)×c(SO32-)<0.1×6.3×10-8=6.3×10-9<Ksp(BaSO3)=5.48×10-7;
故答案为:不能;此时溶液中c(Ba2+)<0.1 mol?L-1,c(SO32-)<6.3×10-8mol?L-1,其浓度商Q=c(Ba2+)×c(SO32-)<0.1×6.3×10-8=6.3×10-9<Ksp(BaSO3)=5.48×10-7;
(2)①A中发生Cu与浓硫酸的反应为Cu+2H2SO4(浓)
| ||
| ||
②C中BaCl2溶液出现白色沉淀的原因为挥发的硫酸与氯化钡反应,故答案为:挥发的硫酸与氯化钡反应;
(3)由实验目的可知,B中发生硫酸与亚硫酸的反应,利用氮气将生成的二氧化硫气体赶到C中除杂,然后利用E吸收二氧化硫,最后连接F防止空气中的水、二氧化碳进入E装置,则按气体流向选用的仪器为BCEF,故答案为:BCEF;
(4)样品质量为m1 g,生成二氧化硫的质量为m2g,亚硫酸钠的质量为
| 63m2 |
| 32 |
| 63m2 |
| 32m1 |
| 63m2 |
| 32m1 |
(5)为减少实验误差,本实验中很重要的操作是反应后要通入氮气一段时间,将装置中生成的二氧化硫全部排入到E装置中,故答案为:反应后要通入氮气一段时间.
点评:本题考查物质含量的测定及实验,为高频考点,把握装置的作用、物质的性质及发生的反应为解答的关键,侧重分析、实验及计算能力的综合考查,注意实验设计的分析,题目难度中等.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
| A、64gSO2中含有的氧原子数为2NA |
| B、同温同压下,相同体积的任何气体所含原子个数相同 |
| C、40gNaOH溶解在1L水中,所制得的溶液,物质的量浓度为1mol?L-1 |
| D、标准状况下,11.2LH2O含有的电子数为5NA |
NaNO2是一种食品添加剂,它能致癌,酸性KMnO4溶液与NaNO2反应的离子方程式为MnO4-+NO2-+H+-Mn2++□+H2O (未配平).下列叙述正确的是( )
| A、反应后溶液pH下降 |
| B、通常用盐酸酸化的高锰酸钾溶液 |
| C、方框中粒子为NO2 |
| D、当生成1 mol Mn2+ 需消耗2.5 mol NO2- |
下列电子排布图中,属于基态碳的是( )
A、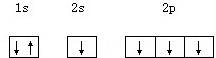 |
B、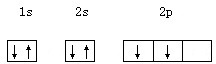 |
C、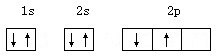 |
D、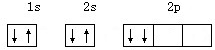 |
若某原子的外围电子排布式为3d14s2,则下列说法正确的是( )
| A、该元素原子中,3d、4s电子的能量逐渐升高 |
| B、该元素位于周期表ds区 |
| C、该元素在元素周期表中的位置为第四周期IIIB族 |
| D、该元素原子最外层有3个电子 |
下列各原子轨道中能容纳电子数最多的是( )
| A、5p | B、6s | C、4f | D、4d |
某合金(仅含铜、铁)中铜和铁的物质的量之和为y mol,其中Cu的物质的量分数为a,将其全部投入50mL b mol?L-1的硝酸溶液中,加热使其充分反应(假设NO是唯一的还原产物).下列说法正确的是( )
| A、若金属有剩余,在溶液中再滴入硫酸后,金属又开始溶解 | ||
| B、若金属全部溶解,则溶液中一定含有Fe3+ | ||
| C、若金属全部溶解,且产生336mL气体(标准状况),则b=0.3 | ||
D、当溶液中金属离子只有Fe3+、Cu2+时,则a与b的关系为:b<80y(1-
|