题目内容
8.有一包粉末,可能是氯化钾、碳酸钠、三氯化铁、硫酸钠、硝酸钡中的一种或几种组成.为了研究它的组成,我做了如下实验,现将研究的问题和实验过程填写在下表中(假设各步恰好完全反应):| 问题 | 实验步骤 | 实验现象 | 结论 | |
实验一 | 存在有色离子吗? | 取少量粉末,加水,溶解,过滤 | 有白色沉淀生成,滤液无色 | 这种粉末中一定无FeCl3 |
实验二 | 白色沉淀是什么? | 取少量沉淀,向其中滴加稀盐酸 | 沉淀部分溶解有气泡产生 | 有硫酸钠、碳酸钠、硝酸钡 |
实验三 | 是否含有KCl? | 取少量滤液,滴加硝酸银溶液和稀硝酸 | 产生白色沉淀 | 有KCl存在 |
分析 根据铁离子在溶液中显黄色,钡离子和碳酸根离子、硫酸根离子会生成沉淀,硫酸钡难溶于酸和水,氯化银沉淀难溶于酸,检验氯离子需要加酸排除碳酸根离子的干扰进行分析.
解答 解:氯化铁在溶液中显黄色,有白色沉淀生成,滤液无色,所以一定不存在氯化铁,可能存在硝酸钡和碳酸钠、硫酸钠,取沉淀滴加盐酸,沉淀全部溶解,依据硫酸钡沉淀难溶于酸,所以沉淀是碳酸钡沉淀,混合物中一定存在碳酸钠和氯化钡,鉴别氯化钾,取实验一反应后的滤液少许,滴加硝酸酸化的硝酸银,会生成白色沉淀,说明存在氯化钾,反之不存在.通过实验推断此粉末的组成是碳酸钠、硝酸钡、氯化钾,要根据这个实验结论完成对现象和步骤的设计.
故答案为:
| 问题 | 实验步骤 | 实验现象 | 结论 | |
| 实验一 | FeCl3 | |||
| 实验二 | 沉淀部分溶解有气泡产生 | 有硫酸钠、碳酸钠、硝酸钡 | ||
| 实验三 | 是否含有KCl? | 取少量滤液,滴加硝酸银溶液和稀硝酸 | 产生白色沉淀 | 有KCl存在 |
点评 本题考查了物质检验和物质性质的分析,在解此类题时,首先分析粉末中各组物质的性质,然后根据题中的现象和自己设计的实验进行分析判断,最后进行汇总即可,题目难度中等.

练习册系列答案
 智能训练练测考系列答案
智能训练练测考系列答案
相关题目
16.下表列出了A~R等9种元素在周期表中的位置;
(1)写出下列元素的名称;A钠,C镁,E碳,R氩.
(2)D的原子结构示意图为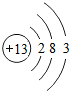 ,其最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
,其最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
(3)A、B、C三种元素的原子半径由大到小的顺序为K>Na>Mg(填元素符号),其最高价氧化物对应水化物的碱性由强到弱顺序为KOH>NaOH>Mg(OH)2.(填化学式)
(4)F元素的氢化物的电子式为 ,其中一种氢化物在常温下与MnO2混合的反应化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
,其中一种氢化物在常温下与MnO2混合的反应化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
(5)用电子式表示A与H形成化合物的过程为 ,高温灼伤该化合物时,火焰呈黄色.
,高温灼伤该化合物时,火焰呈黄色.
| IA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 | |
| 2 | E | F | ||||||
| 3 | A | C | D | G | R | |||
| 4 | B | H |
(2)D的原子结构示意图为
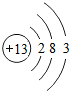 ,其最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.
,其最高价氧化物的水化物与氢氧化钠溶液反应的离子方程式是Al(OH)3+OH-=AlO2-+2H2O.(3)A、B、C三种元素的原子半径由大到小的顺序为K>Na>Mg(填元素符号),其最高价氧化物对应水化物的碱性由强到弱顺序为KOH>NaOH>Mg(OH)2.(填化学式)
(4)F元素的氢化物的电子式为
 ,其中一种氢化物在常温下与MnO2混合的反应化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.
,其中一种氢化物在常温下与MnO2混合的反应化学方程式为2H2O2$\frac{\underline{\;MnO_2\;}}{\;}$2H2O+O2↑.(5)用电子式表示A与H形成化合物的过程为
 ,高温灼伤该化合物时,火焰呈黄色.
,高温灼伤该化合物时,火焰呈黄色.
13.煤是工业的粮食,石油是工业的血液.下列关于煤和石油的说法中错误的是( )
| A. | 石油裂解主要目的是得到短链的不饱和烃 | |
| B. | 煤中含有苯和甲苯,可用先干馏后分馏的方法将它们分离出来 | |
| C. | 煤的气化与液化都是化学变化 | |
| D. | 含C18以上烷烃的重油经过催化裂化可以得到汽油 |
14.下列有关物质的性质与其应用不相对应的是( )
| A. | Al具有良好延展性和抗腐蚀性,可制成铝箔包装物品 | |
| B. | NaHCO3能与碱反应,食品工业用作焙制糕点的膨松剂 | |
| C. | 药皂中加入少量苯酚,可以起到杀菌消毒的作用 | |
| D. | 明矾能水解生成Al(OH)3胶体,可用作净水剂 |
15.下列有关实验的叙述,正确的是( )
| A. | 用瓷坩埚熔融氢氧化钠或碳酸钠 | |
| B. | 用玻璃棒蘸取溶液,点在湿润的pH试纸上测定溶液的pH值 | |
| C. | 取用金属钠、钾时,未用完的钠、钾应放回原瓶 | |
| D. | 读取量筒内液体的体积,俯视读数会导致读数偏小 |
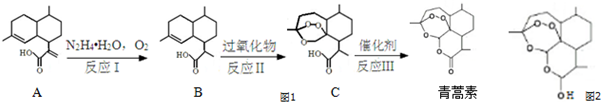
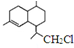 为原料合成B,写出其合成路线(指明所用试剂和反应条件).
为原料合成B,写出其合成路线(指明所用试剂和反应条件).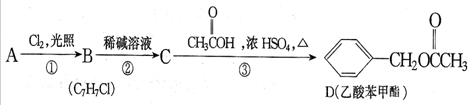
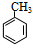 .
.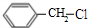 +NaOH$→_{△}^{水}$
+NaOH$→_{△}^{水}$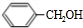 +NaCl.
+NaCl.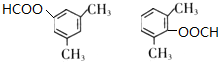 .
.