题目内容
11.某有机物甲在稀硫酸中加热水解生成乙和丙,乙在一定条件下可以转化成丙,下列有关甲的分子式与符合该条件的同分异构体数目的判断中不正确的是( )| 选项 | 分子式 | 同分异构体数目 |
| A | C4H8O2 | 1 |
| B | C6H12O2 | 2 |
| C | C8H16O2 | 3 |
| D | C10H20O2 | 4 |
| A. | A | B. | B | C. | C | D. | D |
分析 某有机物甲在稀硫酸中加热水解生成乙和丙,乙在一定条件下可以转化成丙,说明乙为醇,丙为羧酸,乙、丙的碳原子数相同,且乙中含有-CH2OH,以此解答该题.
解答 解:A、C4H8O2在稀硫酸中加热水解生成乙酸和乙醇,乙醇为CH3CH2OH,乙酸为CH3COOH,-CH3只有一种结构,所以酯只有1种结构,故A正确;
B、C6H12O2在稀硫酸中加热水解生成丙酸和丙醇,丙醇为CH3CH2CH2OH,丙酸为CH3CH2COOH,CH3CH2-只有一种,所以酯有2种结构,故B正确;
C、C8H16O2在稀硫酸中加热水解生成丁酸和丁醇,丁醇为C3H7CH2OH,丁酸为C3H7COOH,而C3H7-有CH3CH2CH2-和CH3CH(CH3)-2种,所以酯有2种结构,故C错误;
D、C10H20O2在稀硫酸中加热水解生成戊酸和戊醇,戊醇为C4H9CH2OH,戊酸为C4H9COOH,-C4H9有:-CH2CH2CH2CH3、-CH(CH3)CH2CH3、-CH2CH(CH3)2、-C(CH3)24种,所以酯有4种结构,故D正确;
故选C;
点评 本题考查同分异构体书写、官能团的结构与性质等,关键是确定醇的结构特点,也利用取代法确定醇的同分异构体.

练习册系列答案
 黄冈小状元解决问题天天练系列答案
黄冈小状元解决问题天天练系列答案 三点一测快乐周计划系列答案
三点一测快乐周计划系列答案
相关题目
15.在花瓶中加入“鲜花保鲜剂”,能延长鲜花的寿命.表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
(1)配制上述“鲜花保鲜剂”所需的仪器有:烧杯、电子天平、药匙、量筒、玻璃棒、500 mL容量瓶、胶头滴管.(在横线上填写所缺仪器的名称)
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
| 成分 | 质量(g) | 摩尔质量(g•mol-1) |
| 蔗糖 | 25.00 | 342 |
| 硫酸钾 | 0.25 | 174 |
| 阿司匹林(C9H8O4) | 0.17 | 180 |
| 高锰酸钾 | 0.25 | 158 |
| 硝酸银 | 0.02 | 170 |
(2)下列“鲜花保鲜剂”的成分中,属于非电解质的是A.(填序号)
A、蔗糖 B、硫酸钾 C、高锰酸钾 D、硝酸银
(3)使用容量瓶前,必须进行的一步操作是检查容量瓶是否漏水.
(4)定容的正确操作是向容量瓶中加水至距离刻度线1-2cm时,改用胶头滴管逐滴加水至液面最低处与刻度线相切.
(5)在溶液配制过程中,下列操作对配制结果没有影响的是BD.
A、定容时俯视容量瓶刻度线
B、容量瓶在使用前未干燥,里面有少量蒸馏水
C、所用过的烧杯、玻璃棒未洗涤
D、定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理.
19.科学家预测原子序数为114的元素,它的位置在第7周期IVA族,称为类铅.关于它的性质,预测错误的是( )
| A. | 它的最外层电子数为4 | B. | 它的金属性比铅强 | ||
| C. | 它具有+2、+4价 | D. | 它的最高价氧化物的水化物是强酸 |
6.在一定温度下,反应A2(气)+B2(气)?2AB(气)达到平衡状态的标志是( )
| A. | 单位时间里消耗n molA2,同时生成2n molAB | |
| B. | 容器中的总压强不随时间而变化 | |
| C. | A2、B2、AB的物质的量之比满足1:2:3 | |
| D. | 单位时间里生成2n molAB的同时生成n molB2 |
16.A、B、C、D、E、F六种元素,其中ABCDE为短周期元素,①原子半径A<C<B<E<D②原子最外层电子数A=D、C=E、A+B=C③原子的核外电子层数B=C=2A④B元素的最高正价与最低负价数值之差为2⑤F在地壳中金属元素含量第二,下列说法正确的是( )
| A. | 因为C的氢化物分子内含有氢键,所以比E的氢化物稳定 | |
| B. | 过量F与氯气加热完全反应,得到相应的低价态氯化物 | |
| C. | 因为E单质相对分子量小于溴单质的相对分子量,所以E单质熔点比溴低 | |
| D. | A、D形成化合物的水溶液呈碱性 |
3.某温度下,反应2N2O5(g)═4NO2(g)+O2(g)开始时,c(N2O5)=0.040 8mol•L-1,经1min后,c(N2O5)=0.030 0mol•L-1.则该反应的反应速率为( )
| A. | v(N2O5)=1.80×10-3 mol•L-1•min-1 | B. | v(N2O5)=1.08×10-2 mol•L-1•min-1 | ||
| C. | v(NO2)=1.80×10-3 mol•L-1•min-1 | D. | v(O2)=1.80×10-2 mol•L-1•min-1 |
20.下列物质互为同分异构体的是( )
| A. | CH3COOH和CH3COOCH3 | B. | CH3CH2OH 和CH3OCH3 | ||
| C. | CH3OCHO和HCOOCH3 | D. | 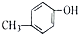 和 和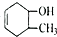 |
1.已知Y元素最高正价与最低负价的绝对值之差是4,Y元素与M元素形成离子化合物,并在水中电离出电子层结构相同的离子,该化合物是( )
| A. | KCl | B. | K2S | C. | Na2S | D. | Na2O |
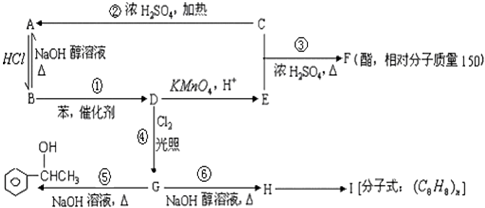
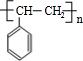
 ;③
;③ +CH3CH2OH$→_{△}^{浓硫酸}$
+CH3CH2OH$→_{△}^{浓硫酸}$ +H2O;⑥
+H2O;⑥ .
.