题目内容
5.把0.2molCO2通入含0.3molNaOH的溶液中,恰好完全反应,求生成Na2CO3和NaHCO3的质量.分析 把0.2molCO2通入含0.3molNaOH的溶液中,分别发生2NaOH+CO2=Na2CO3+H2O、NaOH+CO2=NaHCO3,利用Na、C原子守恒列方程式组进行计算.
解答 解:把0.2molCO2通入含0.3molNaOH的溶液中,分别发生2NaOH+CO2=Na2CO3+H2O、NaOH+CO2=NaHCO3,
设NaHCO3和Na2CO3的物质的量分别是xmol、ymol,利用Na、C原子守恒列方程式组得:
$\left\{\begin{array}{l}{x+y=0.2(C守恒)}\\{x+2y=0.3(H守恒)}\end{array}\right.$,解得$\left\{\begin{array}{l}{x=0.1}\\{y=0.1}\end{array}\right.$,则m(Na2CO3)=0.1mol×106g/mol=10.6g,m(NaHCO3)=0.1mol×84g/mol=8.4g,
答:Na2CO3 为10.6g,NaHCO3 为8.4g.
点评 本题考查混合物的有关计算,侧重考查分析计算能力,利用原子守恒分析解答即可,题目难度不大.

练习册系列答案
相关题目
16.下列离子方程式书写正确的是( )
| A. | 铜和稀硝酸反应 Cu+4H++NO3-=Cu2++2H2O+NO↑ | |
| B. | 碳酸氢钠的水解 HCO3-+H2O?CO32-+H3O+ | |
| C. | Fe投入盐酸中 2Fe+6H+=2Fe3++3H2↑ | |
| D. | 氢氧化铝溶于氢氧化钠溶液 Al(OH)3+OH-=AlO2-+2H2O |
13.将1.4g氮气,1.6g氧气,4g氩气混合,则该混合气体在标准状况下的体积是( )
| A. | 3.36 L | B. | 4.48 L | C. | 6.72 L | D. | 8.96 L |
17.石墨和金刚石都是碳元素的单质,石墨在一定条件下可转化为金刚石.已知12g石墨完全转化成金刚石时,要吸收E kJ的能量,下列说法正确的是( )
| A. | 石墨不如金刚石稳定 | |
| B. | 金刚石不如石墨稳定 | |
| C. | 等质量的石墨与金刚石完全燃烧,金刚石放出的能量少 | |
| D. | 等质量的石墨与金刚石完全燃烧,二者放出的热量相等 |
14.10ml浓度为1mol/L的盐酸与过量的锌粉反应,若加入适量的下列溶液,能减慢反应速率但又不影响氢气生成总量的是( )
①K2SO4 ②CH3COONa ③CuSO4 ④Na2SO4.
①K2SO4 ②CH3COONa ③CuSO4 ④Na2SO4.
| A. | ①③ | B. | ②④ | C. | ①②④ | D. | ③④ |
15.下列各组物质之间,一定互为同系物的是( )
| A. | 乙二醇与丙三醇 | B. | C4H8与C6H12 | ||
| C. | HCOOH与C17H35COOH | D. | 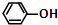 与 与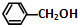 |
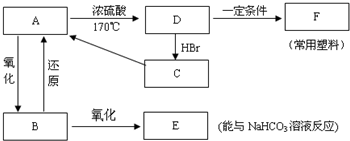
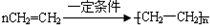 .
. .
.