题目内容
12.根据下列实验操作和现象所得到的结论正确的是( )| 选项 | 实验操作和现象 | 结论 |
| A | 向硝酸溶液中加入碳酸钠,有大量气泡产生 | 酸性:碳酸>硝酸 |
| B | 向1mL 某溶液中,滴入2mL 0.1mol•L-1 NaOH溶液,加热,产生使湿润的红色石蕊试纸变蓝的气体 | 某溶液中含NH4+ |
| C | 取5mL 0.1mol•L-1FeCl3溶液,滴加5滴0.1mol•L-1KI溶液,振荡,再加入5mL CCl4,振荡,静置,取上层液体,向取出来的溶液中滴加KSCN溶液,显血红色. | KI和FeCl3反应有一定的限度 |
| D | 加热使冰化成液态水 | 分子内H-O键发生断裂 |
| A. | A | B. | B | C. | C | D. | D |
分析 A.发生强酸制取弱酸的反应;
B.使湿润的红色石蕊试纸变蓝的气体为氨气;
C.滴加5滴0.1mol•L-1KI溶液,20滴约为1mL,氯化铁有剩余;
D.加热使冰化成液态水,为物理变化,只破坏分子间作用力.
解答 解:A.向硝酸溶液中加入碳酸钠,有大量气泡产生,发生强酸制取弱酸的反应,则酸性:硝酸>碳酸,故A错误;
B.使湿润的红色石蕊试纸变蓝的气体为氨气,则某溶液中含NH4+,故B正确;
C.滴加5滴0.1mol•L-1KI溶液,20滴约为1mL,氯化铁有剩余,则取出来的溶液中滴加KSCN溶液,显血红色,不能说明KI和FeCl3反应有一定的限度,故C错误;
D.加热使冰化成液态水,为物理变化,只破坏分子间作用力,而分子内H-O键不变,故D错误;
故选B.
点评 本题考查化学实验方案的评价,为高频考点,把握物质的性质、离子检验、化学键、反应限度为解答的关键,侧重分析与实验能力的考查,注意实验的评价性分析,题目难度不大.

练习册系列答案
相关题目
17.下列化学用语表述正确的是( )
| A. | 氯气的电子式: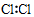 | B. | 氮气的结构式: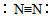 | ||
| C. | F一的结构示意图: | D. | H2O2的电子式: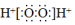 |
4.设NA为阿伏加德罗常数的值,则下列说法正确的是( )
| A. | 标准状况下,2.24 LCCl4中含Cl原子数目为0.4NA | |
| B. | 28g聚乙烯中所含原子数为6NA | |
| C. | 0.1mol苯乙烯中含有双键的数目为0.4NA | |
| D. | 常温常压下,10 g 46%酒精水溶液中含氧原子总数为0.1NA |
1.对增生性瘢痕早期进行${\;}_{38}^{90}$Sr(锶)干预可取得较好效果.下列说法正确的是( )
| A. | Sr为于第4周期ⅡA 族 | |
| B. | ${\;}_{38}^{90}$Sr核内中子数与质子数之差为14 | |
| C. | ${\;}_{38}^{90}$Sr与${\;}_{39}^{90}$Y互为同位素 | |
| D. | ${\;}_{38}^{90}$Sr的核内质子数为38,Sr元素的相对原子质量为90 |

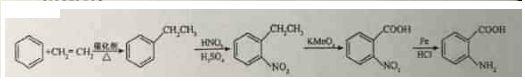
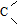 →-N=
→-N=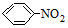 $\stackrel{Fe/HCl}{→}$
$\stackrel{Fe/HCl}{→}$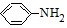 (易被氧化).请回答:
(易被氧化).请回答: ;
;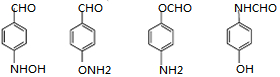 ;
; .
.