题目内容
20.硫酸法是现代氧化铍或氢氧化铍生产中广泛应用的方法之一,其原理是利用预焙烧破坏铍矿物(绿柱石-3BeO•Al2O3•6SiO2及少量FeO等)的结构与晶型,再采用硫酸酸解含铍矿物,使铍、铝、铁等酸溶性金属进入溶液相,与硅等脉石矿物初步分离,然后将含铍溶液进行净化、除杂,最终得到合格的氧化铍( 或氢氧化铍) 产品,其 工艺流程如图.
工艺流程如图.已知:(1)铝铵矾的化学式是NH4Al(SO4)2•12H2O
(2)铍元素的化学性质与铝元素相似
根据以上信息回答下列问题:
(1)熔炼物酸浸前通常要进行粉碎,其目的是:提高铍元素的浸出速率和浸出率.
(2)“蒸发结晶离心除铝”若在中学实验室中进行,完整的操作过程是蒸发浓缩、冷却结晶洗涤、过滤.
(3)“中和除铁”过程中“中和”所发生反应的离子方程式是H++NH3•H2O=NH4++H2O,用平衡原理解释“除铁”的过程由于存在平衡Fe3++3H2O?Fe(OH)3+3H+,氨水中和H+,使c(H+)减小,上述平衡正向移动,使Fe3+转化为Fe(OH)3沉淀而除去.
(4)加入的“熔剂”除了流程中的方解石外,还可以是纯碱、石灰等.其中,石灰具有价格与环保优势,焙烧时配料比( m石灰/m绿柱石) 通常控制为1:3,焙烧温度一般为1400℃-1500℃.若用纯碱作熔剂,SiO2与之反应的化学方程式是SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑,若纯碱加入过多则Al2O3、BeO2也会发生反应,其中BeO与之反应的化学方程式是BeO+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2BeO2+CO2↑,从而会导致酸浸时消耗更多硫酸,使生产成本升高,结合离子方程式回答成本升高的原因由BeO+2H+=Be2++H2O和BeO22-+4H+=Be2++2H2O可知,BeO转化为BeO22-后将消耗更多硫酸.
分析 铍矿物(绿柱石-3BeO•Al2O3•6SiO2及少量FeO等)和方解石熔炼,然后加入稀硫酸,SiO2、Al2O3分别与CaCO3反应生成CaSiO3、铝酸钙,BeO和熔融方解石反应生成铍酸钙,FeO被氧化,然后加入稀硫酸溶解,浸出出液中含有BeSO4、Al2(SO4)3、Fe2(SO4)3,向滤液中加入硫酸铵,硫酸铝和硫酸铵反应生成NH4Al(SO4)2,通过离心沉淀得到NH4Al(SO4)2•12H2O,滤液中含有BeSO4、(NH4)2SO4、Fe2(SO4)3,然后向溶液中加入氨水,调节溶液pH除去铁离子,然后过滤得到氢氧化铁沉淀,滤液中含有BeSO4,再向溶液中加入氨水,得到Be(OH)2沉淀,煅烧氢氧化铍得到工业BeO,
(1)增大反应物接触面积,增大反应速率;
(2)“蒸发结晶离心除铝”若在中学实验室中进行,完整的操作过程蒸发浓缩、冷却结晶、洗涤、过滤;
(3)“中和除铁”过程中“中和”实质上是利用氨水和溶液中氢离子反应促进铁离子水解;
(4)高温条件下,碳酸钠和二氧化硅反应生成硅酸钠和二氧化碳;高温条件下,BeO和碳酸钠反应生成铍酸钠和二氧化碳,BeO转化为BeO22-后将消耗更多硫酸.
解答 解:铍矿物(绿柱石-3BeO•Al2O3•6SiO2及少量FeO等)和方解石熔炼,然后加入稀硫酸,SiO2、Al2O3分别与CaCO3反应生成CaSiO3、铝酸钙,BeO和熔融方解石反应生成铍酸钙,FeO被氧化,然后加入稀硫酸溶解,浸出出液中含有BeSO4、Al2(SO4)3、Fe2(SO4)3,向滤液中加入硫酸铵,硫酸铝和硫酸铵反应生成NH4Al(SO4)2,通过离心沉淀得到NH4Al(SO4)2•12H2O,滤液中含有BeSO4、(NH4)2SO4、Fe2(SO4)3,然后向溶液中加入氨水,调节溶液pH除去铁离子,然后过滤得到氢氧化铁沉淀,滤液中含有BeSO4,再向溶液中加入氨水,得到Be(OH)2沉淀,煅烧氢氧化铍得到工业BeO,
(1)增大反应物接触面积,增大反应速率,所以将熔炼物酸浸前通常要进行粉碎,其目的是提高铍元素的浸出速率和浸出率,故答案为:提高铍元素的浸出速率和浸出率;
(2)“蒸发结晶离心除铝”若在中学实验室中进行,完整的操作过程蒸发浓缩、冷却结晶、洗涤、过滤,
故答案为:蒸发浓缩、冷却结晶;
(3)“中和除铁”过程中“中和”实质上是利用氨水和溶液中氢离子反应,离子方程式为H++NH3•H2O=NH4++H2O;由于存在平衡Fe3++3H2O?Fe(OH)3+3H+,氨水中和H+,使c(H+)减小,上述平衡正向移动,使Fe3+转化为Fe(OH)3沉淀而除去,
故答案为:H++NH3•H2O=NH4++H2O;由于存在平衡Fe3++3H2O?Fe(OH)3+3H+,氨水中和H+,使c(H+)减小,上述平衡正向移动,使Fe3+转化为Fe(OH)3沉淀而除去;
(4)高温条件下,碳酸钠和二氧化硅反应生成硅酸钠和二氧化碳,反应方程式为SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑;高温条件下,BeO和碳酸钠反应生成铍酸钠和二氧化碳,反应方程式为BeO+Na2CO3$\frac{\underline{\;高温\;}}{\;}$ Na2BeO2+CO2↑,由BeO+2H+=Be2++H2O和BeO22-+4H+=Be2++2H2O可知,BeO转化为BeO22-后将消耗更多硫酸,
故答案为:SiO2+Na2CO3$\frac{\underline{\;高温\;}}{\;}$Na2SiO3+CO2↑;BeO+Na2CO3$\frac{\underline{\;高温\;}}{\;}$ Na2BeO2+CO2↑;由BeO+2H+=Be2++H2O和BeO22-+4H+=Be2++2H2O可知,BeO转化为BeO22-后将消耗更多硫酸.
点评 本题考查物质分离和提纯,为高频考点,综合性较强,涉及离子方程式及化学方程式的书写、化学反应速率影响因素、分离提纯基本操作、盐类水解等知识点,明确反应原理及流程图中每一步发生的反应、采用的操作方法是解本题关键,题目难度中等.

| A. | Al2O3难溶于水,不跟水反应,所以它不是Al(OH)3对应的氧化物 | |
| B. | 因为Al2O3是金属氧化物,所以它是碱性氧化物 | |
| C. | Al2O3属于两性氧化物 | |
| D. | Al2O3能与所有的酸、碱溶液反应 |
| A. |  除去CO中的CO2 | B. | 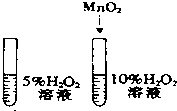 探究二氧化锰对反应速率的影响 | ||
| C. | 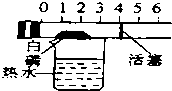 探究空气中氧气的含量 | D. |  探究溶解性的影响因素 |
| A. | Ba2+、Al3+、SO42-、NO3- | B. | Mg2+、K+、Cl-、NO3- | ||
| C. | HCO3-、K+、Cu2+、SO42- | D. | K+、Na+、OH-、Br |
| A. | Na投入到水中:Na+H2O═Na++OH-+H2↑ | |
| B. | AlCl3溶液中加入足量的氨水:Al3++3OH-═Al(OH)3↓ | |
| C. | Al2O3和NaOH溶液:Al2O3+2OH-═2AlO2-+H2O | |
| D. | FeCl2溶液跟Cl2反应:Fe2++Cl2═Fe3++2Cl- |
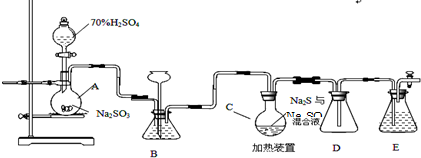
 如图是用浓硝酸、稀硝酸、铜片、水等试剂探究浓、稀硝酸的强氧化性并观察还原产物的实验装置.
如图是用浓硝酸、稀硝酸、铜片、水等试剂探究浓、稀硝酸的强氧化性并观察还原产物的实验装置.