题目内容
碳酸钠、碳酸氢钠、淀粉在工业生产、食品加工具有广泛的用途.请回答下列问题:
(1)在家庭厨房检验碳酸钠、碳酸氢钠的试剂或方法是 .
A.加热 B.食醋 C.食盐D.矿泉水
(2)如果厨房没有小苏打而有苏打,怎样制取小苏打 ,化学方程式为 .
(3)苏打对硬水有软化作用,化学方程式为 .
(4)用小苏打溶液加果汁加柠檬酸可自制汽水,是利用 产生CO2.
(1)在家庭厨房检验碳酸钠、碳酸氢钠的试剂或方法是
A.加热 B.食醋 C.食盐D.矿泉水
(2)如果厨房没有小苏打而有苏打,怎样制取小苏打
(3)苏打对硬水有软化作用,化学方程式为
(4)用小苏打溶液加果汁加柠檬酸可自制汽水,是利用
考点:常见的食品添加剂的组成、性质和作用
专题:化学应用
分析:(1)碳酸钠与少量醋酸反应生成碳酸氢钠;
(2)苏打俗称纯碱,可以跟CO2和H2O反应生成NaHCO3;
(3)碳酸钠能与氯化钙反应生成碳酸钙沉淀;
(4)柠檬酸酸性比碳酸强;
(2)苏打俗称纯碱,可以跟CO2和H2O反应生成NaHCO3;
(3)碳酸钠能与氯化钙反应生成碳酸钙沉淀;
(4)柠檬酸酸性比碳酸强;
解答:
解:(1)碳酸钠与少量醋酸反应生成碳酸氢钠,碳酸氢钠与醋酸反应生成二氧化碳,滴入醋酸立即有气体的是碳酸氢钠,故答案为:B;
(2)反应物为Na2CO3、CO2和H2O;生成物为NaHCO3,根据质量守恒定律:Na2CO3+CO2+H2O═2NaHCO3,故答案为:通入二氧化碳;Na2CO3+CO2+H2O═2NaHCO3;
(3)碳酸钠能与氯化钙反应生成碳酸钙沉淀,化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,故答案为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
(4)柠檬酸酸性比碳酸强,碳酸氢钠与酸反应生成二氧化碳,故答案为:碳酸氢钠与酸反应.
(2)反应物为Na2CO3、CO2和H2O;生成物为NaHCO3,根据质量守恒定律:Na2CO3+CO2+H2O═2NaHCO3,故答案为:通入二氧化碳;Na2CO3+CO2+H2O═2NaHCO3;
(3)碳酸钠能与氯化钙反应生成碳酸钙沉淀,化学方程式为:Na2CO3+CaCl2=CaCO3↓+2NaCl,故答案为:Na2CO3+CaCl2=CaCO3↓+2NaCl;
(4)柠檬酸酸性比碳酸强,碳酸氢钠与酸反应生成二氧化碳,故答案为:碳酸氢钠与酸反应.
点评:本题考查化学与生活,为高考常见题型和高频考点,有利于培养学生的良好科学素养,难度不大,注意相关基础知识的积累.

练习册系列答案
相关题目
下列物质鉴别的方法正确的是( )
| A、用焰色反应鉴别氯化钠固体和氢氧化钠固体 |
| B、用丁达尔效应鉴别NaCl溶液和KCl溶液 |
| C、用AgNO3溶液鉴别NaCl溶液和Na2SO4溶液 |
| D、用萃取法鉴别溴水和碘水 |
下列各组离子一定可以大量共存的是( )
| A、在含大量Al3+的溶液中:NH4+、Na+、HCO3-、SO42- |
| B、能使甲基橙试液变红的溶液中:Na+、K+、MnO4-、NO3- |
| C、在水电离出的c(H+)=10-13mol?L-1 的溶液中:NH4+、[Al(OH)4]-、SO42-、NO3- |
| D、在pH=1的溶液中:K+、Fe2+、Cl-、NO3- |
下列每组中各有三种混合物,它们都能用分液漏斗分离的是( )
| A、乙酸乙酯和水,酒精和水,植物油和水 |
| B、甘油和水,乙酸和水,乙酸和乙醇 |
| C、四氯化碳和水,溴苯和水,硝基苯和水 |
| D、汽油和水,苯和水,乙醛和水 |
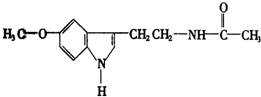 “今年过节不收礼,收礼还收脑白金”,反应了中国人收礼的习俗,脑白金中有效成分的结构简式如图,下列对该化合物的叙述正确的是( )
“今年过节不收礼,收礼还收脑白金”,反应了中国人收礼的习俗,脑白金中有效成分的结构简式如图,下列对该化合物的叙述正确的是( )| A、它属于芳香烃,含有碳碳双键和肽键,能使高锰酸钾溶液和溴水褪色,但原理不同 |
| B、它属于高分子化合物,所有原子不可能共面 |
| C、分子式C13N2H16O2,能和盐酸发生化学反应,体现了一定的碱性 |
| D、在一定条件下可以发生加成反应、氧化反应、水解反应,不能发生酯化反应 |
在①丙烯 ②四氟乙烯 ③氯苯 ④环已烯 四种有机化合物中,分子内所有原子均在同一平面的是( )
| A、①② | B、②④ | C、③④ | D、②③ |
