题目内容
16.下列盛放试剂或取用试剂的方法,正确的是( )| A. | 浓硝酸或氢氟酸存放在配有磨口塞的棕色玻璃瓶中 | |
| B. | 汽油或煤油存放在带橡皮塞的棕色玻璃瓶中 | |
| C. | 用碱式滴定管准确量取25.00mL的KMnO4溶液 | |
| D. | 新制氯水或硝酸银溶液存放在配有磨口塞的棕色玻璃瓶中 |
分析 A.氢氟酸与玻璃中的二氧化硅反应;
B.汽油或煤油等有机溶剂易使橡胶溶解而膨胀;
C.高锰酸钾腐蚀橡胶管;
D.次氯酸、硝酸银见光易分解.
解答 解:A.玻璃中含有二氧化硅,与氢氟酸反应,不能用玻璃瓶盛放氢氟酸,故A错误;
B.汽油或煤油等有机溶剂易使橡胶溶解而膨胀,因而不能用橡胶塞,故B错误;
C.碱式滴定管有橡胶管,而高锰酸钾腐蚀橡胶管,应用酸式滴定管,故C错误;
D.氯水中含有次氯酸,次氯酸、硝酸银见光易分解,应存放在配有磨口塞的棕色玻璃瓶中,故D正确.
故选D.
点评 本题以药品的存放为载体综合考查元素化合物知识,侧重于学生的分析、实验能力的考查,注意把握物质的性质以及实验的合理性的评价,难度不大.

练习册系列答案
 海淀黄冈名师导航系列答案
海淀黄冈名师导航系列答案 普通高中同步练习册系列答案
普通高中同步练习册系列答案
相关题目
7.工业上以锂辉石(Li2O•A12O3•4SiO2,含少量Ca、Mg元素)为原料生产碳酸锂.其部分工艺流程如下:
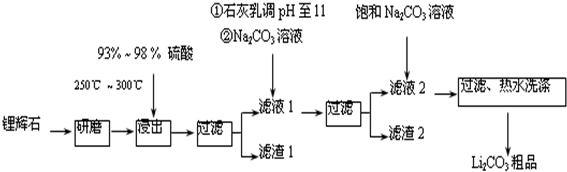
已知:①Li2O•Al2O3•4SiO2+H2SO4(浓)$\frac{\underline{\;250℃-300℃\;}}{\;}$Li2SO4+Al2O3•4SiO2•H2O↓
②某些物质的溶解度(S)如表所示.
(1)从滤渣1中分离出Al2O3的部分流程如图所示,括号表示加入的试剂,方框表示所得到的物质.则步骤Ⅱ中反应的离子方程式是Al3++3NH3•H2O=Al(OH)3↓+3NH4+.
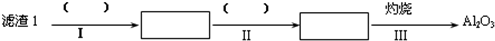
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3.
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)增加Ca2+、OH-的浓度,有利于Mg(OH)2、CaCO3的析出.
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失.
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下.
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3.
①a中,阳极的电极反应式是2C1--2e-=Cl2↑.
②b中,生成Li2CO3反应的化学方程式是2LiOH+NH4HCO3=Li2CO3+NH3+2H2O.

已知:①Li2O•Al2O3•4SiO2+H2SO4(浓)$\frac{\underline{\;250℃-300℃\;}}{\;}$Li2SO4+Al2O3•4SiO2•H2O↓
②某些物质的溶解度(S)如表所示.
| T/℃ | 20 | 40 | 60 | 80 |
| S(Li2CO3)/g | 1.33 | 1.17 | 1.01 | 0.85 |
| S(Li2SO4)/g | 34.2 | 32.8 | 31.9 | 30.7 |
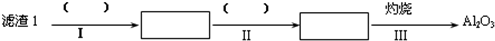
(2)已知滤渣2的主要成分有Mg(OH)2和CaCO3.
向滤液1中加入石灰乳的作用是(运用化学平衡移动原理解释)增加Ca2+、OH-的浓度,有利于Mg(OH)2、CaCO3的析出.
(3)向滤液2中加入饱和Na2CO3溶液,过滤后,用“热水洗涤”的原因是Li2CO3的溶解度随温度升高而减小,热水洗涤可减少Li2CO3的损失.
(4)工业上,将Li2CO3粗品制备成高纯Li2CO3的部分工艺如下.
a.将Li2CO3溶于盐酸作电解槽的阳极液,LiOH溶液作阴极液,两者用离子选择透过膜隔开,用惰性电极电解.
b.电解后向LiOH溶液中加入过量NH4HCO3溶液,过滤、烘干得高纯Li2CO3.
①a中,阳极的电极反应式是2C1--2e-=Cl2↑.
②b中,生成Li2CO3反应的化学方程式是2LiOH+NH4HCO3=Li2CO3+NH3+2H2O.
11.下列反应中,属于吸热反应的是( )
| A. | 硝酸铵溶于水 | B. | 氢气在氯气中燃烧 | ||
| C. | 盐酸和氢氧化钠溶液反应 | D. | Ba(OH)2•8H2O与NH4Cl反应 |
1.下列化合物电子式表示不正确的是( )
| A. |  | B. |  | C. |  | D. |  |
8.下列反应对应的离子方程式书写正确的是( )
| A. | 饱和碳酸钠溶液中通入足量的二氧化碳:2Na++CO32-+CO2+H2O═2NaHCO3↓ | |
| B. | FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| C. | NaHSO4溶液中滴入少量Ba(OH)2溶液:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 饱和石灰水与醋酸溶液混合:Ca(OH)2+2CH3COOH═Ca2++2CH3COO-+2H2O |
5.NA代表阿伏加德罗常数,下列说法正确的是( )
| A. | 含NA个H的H2的物质的量为1 mol | |
| B. | NA个CO和1 mol N2所含分子数相等 | |
| C. | NA个H2SO4与1 mol H3PO4所含氢原子的个数比为1:1 | |
| D. | 0.1 mol C含1.2NA个质子 |