题目内容
18.下列元素中,最高正化合价数值最大的是( )| A. | C | B. | F | C. | S | D. | Na |
分析 元素的原子核外最外层电子数决定元素最高化合价,最外层电子数越多,化合价越大,根据最外层电子数判断最高化合价,以此解答该题.
解答 解:A.C的最外层电子数为4,最高化合价为+4价;
B.F无正价;
C.S的最外层电子数为6,最高化合价为+6价;
D.Na的最外层电子数为1,最高化合价为+1价,
则化合价最高的为S.
故选C.
点评 本题考查化合价的判断,为高频考点,侧重考查双基知识,题目难度不大,本题注意根据元素在周期表中的位置可判断最外层电子数,根据最外层电子数判断化合价.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
9.下列根据实验操作和实验现象所得出的结论,正确的是( )
| 选项 | 实验操作 | 实验现象 | 结论 |
| A | 向两份蛋白质溶液中分别滴加饱 和Na2SO4溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生 变性 |
| B | 在CuSO4溶液中加入KI溶液,再 加入苯,振荡后静置 | 有白色沉淀生成,苯层 呈紫红色 | 白色沉淀可能 为CuI |
| C | 将气体X通入品红溶液中 | 红色褪去 | X一定是SO2 |
| D | 将Fe(NO3)2样品溶于稀H2SO4后, 滴加KSCN溶液 | 溶液变为血红色 | Fe(NO3)2样品 已氧化变质 |
| A. | A | B. | B | C. | C | D. | D |
6.2014年《RSC Advances》报道了一种全陶瓷固体氧化物铁-空气电池,工作原理如图所示:

下列说法正确的是( )

下列说法正确的是( )
| A. | 该电池常温下可稳定工作 | |
| B. | 放电时,电能转变为化学能 | |
| C. | 充电时,阳极发生反应:4OH--4e-═2H2O+O2↑ | |
| D. | 放电时,负极室发生反应:Fe+xH2O(g)$\frac{\underline{\;\;△\;\;}}{\;}$FeOx+xH2,负极发生反应:H2+O2--2e-=H2O |
13.常温下,下列溶液中各组离子一定能大量共存的是( )
| A. | 使甲基橙呈红色的溶液:Na+、AlO2-、NO3-、CO32- | |
| B. | 由水电离产生的c(H+)=10-12mol•L-1的溶液:NH4+、SO42-、HCO3-、Cl- | |
| C. | $\frac{{K}_{w}}{c({H}^{+})}$=0.1 mol•L-1的溶液:Na+、K+、CO32-、NO3- | |
| D. | 含有0.1 mol•L-1 HCO3-全部的溶液:Na+、Fe3+、NO3-、SCN- |
3.元素X和Y是同周期主族元素,X元素在第ⅠA族,Y元素在第ⅦA族,则X和Y两元素原子序数之差不可能是( )
| A. | 6 | B. | 16 | C. | 26 | D. | 30 |
10.常温下,下列物质能用铝制器皿盛放的是( )
| A. | 稀硫酸 | B. | 氢氧化钠溶液 | C. | 稀硝酸 | D. | 浓硝酸 |
7.下列不能证明Cl元素的非金属性强于S元素的是( )
| A. | HCl的稳定性强于H2S | |
| B. | Cl元素最高正价为+7,而S元素最高正价为+6 | |
| C. | 将Cl2通入Na2S溶液中,产生黄色沉淀 | |
| D. | 单质与H2化合所需的反应条件,S比Cl2苛刻 |
7.海带是一种富含生物碘的海洋植物,碘是人体必需的微量元素,人体内碘的含量直接影响身体健康,为了防止缺碘,通常向食盐中加入碘酸钾(KIO3),以补充人体对碘的需求.各物质的密度、沸点如下表所示,图1为某兴趣小组从海带中提取碘单质的过程.
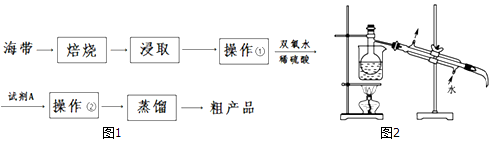
回答下列问题:
(1)实验室焙烧海带时,用不到的仪器有CE (填选项字母).
A.泥三角 B.三脚架 C.烧杯 D.坩埚 E.蒸发皿 F.酒精灯
(2)向浸取液中加入足量的双氧水和稀硫酸时,发生反应的离子方程式为2I-+H2O2+2H+═I2+2H2O.
(3)操作①中除用到玻璃棒外,还需要的玻璃仪器有烧杯、漏斗.
(4)试剂A的名称为四氯化碳 (从上表给出的试剂中选择).
(5)图2是进行蒸馏时的部分仪器,图中缺少的玻璃仪器的名称是温度计、锥形瓶.
(6)工业上可用碘制取碘酸钾,其反应为I2+2KClO3═2KIO3+Cl2↑,下列有关叙述不正确的是A (填选项字母).
A.氧化性:I2>Cl2
B.每生成1mol KIO3,转移5mol e-
C.该反应是置换反应
D.反应物和生成物中均含有共价键.
| 物质 | 乙醇 | 四氯化碳 | 裂化汽油 | 碘(晶体) |
| 密度/g•cm-3 | 0.789 | 1.595 | 0.71~0.76 | 4.93 |
| 沸点/℃ | 78.5 | 76.8 | 25~232 | 184.35 |

回答下列问题:
(1)实验室焙烧海带时,用不到的仪器有CE (填选项字母).
A.泥三角 B.三脚架 C.烧杯 D.坩埚 E.蒸发皿 F.酒精灯
(2)向浸取液中加入足量的双氧水和稀硫酸时,发生反应的离子方程式为2I-+H2O2+2H+═I2+2H2O.
(3)操作①中除用到玻璃棒外,还需要的玻璃仪器有烧杯、漏斗.
(4)试剂A的名称为四氯化碳 (从上表给出的试剂中选择).
(5)图2是进行蒸馏时的部分仪器,图中缺少的玻璃仪器的名称是温度计、锥形瓶.
(6)工业上可用碘制取碘酸钾,其反应为I2+2KClO3═2KIO3+Cl2↑,下列有关叙述不正确的是A (填选项字母).
A.氧化性:I2>Cl2
B.每生成1mol KIO3,转移5mol e-
C.该反应是置换反应
D.反应物和生成物中均含有共价键.