题目内容
Cl2合成有机物时会产生副产物HCl.4HCl+O2
2Cl2+2H2O,可实现氯的循环利用.该反应平衡常数的表达式K为 ;若反应容器的容积为2L,8min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则HCl的平均反应速率为 mol/(L?min).
| CuO/CuCl |
| 400℃ |
考点:化学平衡常数的含义,反应速率的定量表示方法
专题:化学平衡专题
分析:平衡常数指一定温度下到达平衡时,生成物浓度化学计量数次数幂之积与反应物浓度化学计量数次数幂之积的比值;
根据差量法计算参加反应的HCl的物质的量,再根据v=
计算v(HCl).
根据差量法计算参加反应的HCl的物质的量,再根据v=
| ||
| △t |
解答:
解:可逆反应4HCl(g)+O2(g)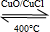 2Cl2(g)+2H2O(g)的平衡常数k=
2Cl2(g)+2H2O(g)的平衡常数k=
;
反应容器的容积为2L,8min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则:
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g) 物质的量减少
4 4+1-2-2=1
n(HCl) 2.5mol-2.25mol=0.25mol
故n(HCl)=
=1mol,
则v(HCl)=
=0.0625mol/(L.min),
故答案为:
;0.0625.
 2Cl2(g)+2H2O(g)的平衡常数k=
2Cl2(g)+2H2O(g)的平衡常数k=| c2(Cl2)?c2(H2O) |
| c4(HCl)?c(O2) |
反应容器的容积为2L,8min后达到平衡,测得容器内物质由2.5mol减少至2.25mol,则:
4HCl(g)+O2(g)?2Cl2(g)+2H2O(g) 物质的量减少
4 4+1-2-2=1
n(HCl) 2.5mol-2.25mol=0.25mol
故n(HCl)=
| 4×0.25mol |
| 1 |
则v(HCl)=
| ||
| 8min |
故答案为:
| c2(Cl2)?c2(H2O) |
| c4(HCl)?c(O2) |
点评:本题考查化学平衡常数、反应速率计算,比较基础,注意利用差量法计算参加反应的HCl的物质的量.

练习册系列答案
 全能测控一本好卷系列答案
全能测控一本好卷系列答案
相关题目
下列物质分类正确的是( )
| A、干冰-氧化物 |
| B、碘酒-单质 |
| C、纯碱-碱 |
| D、葡萄糖-酸 |
下列反应的离子方程式的书写正确的是( )
| A、盐酸与氢氧化钠溶液反应:H++OH-=H2O |
| B、锌粒与稀醋酸反应:Zn+2H+=Zn2++H2↑ |
| C、氯化镁溶液与氨水反应:Mg2++2OH-=Mg(OH)2↓ |
| D、氯气与氢氧化钠溶液反应:Cl2+OH-=Cl-+ClO-+H2O |
 )是一种重要的有机化工原料.
)是一种重要的有机化工原料.
