题目内容
14.下列各组物质的燃烧热相等的是( )| A. | C和CO | B. | 1moC和2moC | C. | 1moC2H2和2molC | D. | SO2和CO2 |
分析 燃烧热是指1 mol物质完全燃烧生成稳定氧化物时所放出的热量,一般C→CO2,H→H2O(l),S→SO2.燃烧热是物质的性质,与量的多少无关,据此进行判断.
解答 解:A、C、D物质不同,具有不同的能量,燃烧热不相等.燃烧热是物质的性质,与量的多少无关,故B正确,
故选B.
点评 本题考查燃烧热的概念及应用,题目难度较小,明确燃烧热的概念为解答关键,试题侧重基础知识的考查,培养了学生的分析能力及灵活应用能力.

练习册系列答案
相关题目
4.在氢氧化钾溶液中,已知钾离子与水分子的物质的量之比为a:b,溶液的密度为ρg/cm3,则溶液的浓度为( )
| A. | $\frac{39a}{18b+39a}×100%$ | B. | $\frac{1000ρa}{56a+18b}mol/L$ | ||
| C. | $\frac{a}{56a+18b}mol/L$ | D. | $\frac{56a}{56a+18b}%$ |
5.短周期主族元素X、Y、Z、M、N的原子序数依次增大.X与M的原子核外最外层电子数是周期数的二倍,Y、Z、M最高价氧化物对应的水化物两两之间能相互反应.下列叙述正确的是( )
| A. | 元素非金属性由弱到强的顺序:M、N、Y | |
| B. | 单质Y的熔点高于单质Z的熔点 | |
| C. | 原子最外层电子数由少到多的顺序:Y、Z、X、M、N | |
| D. | 电解N和Z形成的化合物可得到对应的N和Z的单质 |
2.下列说法不正确的是( )
| A. | 某有机物的结构简式如图所示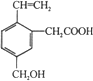 ,该物质属于芳香族化合物是苯的含氧衍生物,含有两种含氧官能团 ,该物质属于芳香族化合物是苯的含氧衍生物,含有两种含氧官能团 | |
| B. | 按系统命名法,有机物(CH3)2CHCH(CH2CH3)(CH2CH2CH3)的命名为:2-甲基-3-乙基己烷 | |
| C. | 总质量一定时,乙炔和乙醛(CH3CHO)无论按什么比例混合,完全燃烧消耗氧气量或生成CO2量不变 | |
| D. | 丙烯酸(CH2═CHCOOH)和山梨酸(CH3CH═CHCH═CHCOOH)不是同系物,它们与氢气充分反应后的产物才是同系物 |
9.在一定温度下的定容容器中,发生反应:2A(g)+B(s)?C(g)+D(g),下列描述中能表明反应已达到平衡状态的是( )
①混合气体的压强不变
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④C(g)的物质的量浓度不变
⑤容器内A、C、D三种气体的浓度之比为2:1:1
⑥单位时间内生成n molD,同时生成2n mol A
⑦单位时间内生成n molC,同时消耗n molD.
①混合气体的压强不变
②混合气体的密度不变
③混合气体的平均相对分子质量不变
④C(g)的物质的量浓度不变
⑤容器内A、C、D三种气体的浓度之比为2:1:1
⑥单位时间内生成n molD,同时生成2n mol A
⑦单位时间内生成n molC,同时消耗n molD.
| A. | ①②③ | B. | ②③④⑥⑦ | C. | ②③⑤⑥⑦ | D. | ①③⑤⑦ |
6.如表中的实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 向含有KSCN溶液的FeSO4溶液中滴加硫酸酸化的H2O2溶液 | 检验H2O2的氧化性大于Fe3+ |
| B | 滴入KI试液 | 检验淀粉是否已完全水解 |
| C | 先滴入Ba(NO3)2溶液.产生沉淀,加入足量稀盐酸,仍有沉淀 | 检验溶液中是否含有SO42- |
| D | 向乙醇溶液加入钠粒 | 测定乙醇分子中含有羟基 |
| A. | A | B. | B | C. | C | D. | D |
3.阿波罗宇宙飞船上使用的是氢氧燃料电池,其电池反应为:2H2+O2=2H2O,电解液为KOH.下列叙述正确的是( )
| A. | 此电池能发出蓝色火焰 | |
| B. | H2为正极,O2为负极 | |
| C. | 工作时,电解液的pH不断增大 | |
| D. | 此电池反应只生成水,对环境没有污染 |
4.N2和O2组成的混合气体,其平均相对分子质量为29,则混合气体中,N2和O2的物质的量之比为( )
| A. | 3:1 | B. | 2:1 | C. | 1:1 | D. | 1:3 |
 ,A的结构简式CH2=CH2.
,A的结构简式CH2=CH2. ,反应类型取代反应.
,反应类型取代反应.