题目内容
20.据《本草纲日》记载:“生熟铜皆有青,即是铜之精华,大者即空绿,以次空青也.铜青则是铜器上绿色者,淘洗用之.”这里的”铜青”是指( )| A. | CuO | B. | Cu20 | C. | Cu | D. | Cu(OH)2CO3 |
分析 Cu与空气中氧气、二氧化碳、水反应生成的,反应方程式为2Cu+O2+H2O+CO2=Cu2(OH)2CO3,据此进行解答.
解答 解:铜在空气中长时间放置,会与空气中氧气、二氧化碳、水反应生成碱式碳酸铜Cu2(OH)2CO3,发生反应为:2Cu+O2+H2O+CO2=Cu2(OH)2CO3,则这里的”铜青”是指Cu2(OH)2CO3,
故选D.
点评 本题考查了铜及其化合物性质,题目难度不大,明确铜长时间在空气中与氧气、二氧化碳和水发生的反应为解答关键,试题侧重基础知识的考查,培养了学生的灵活应用能力.

练习册系列答案
相关题目
10.下列关于胶体的说法中,正确的是( )
| A. | 胶体一定是均一、透明、介稳的 | B. | 用丁达尔效应区别胶体和溶液 | ||
| C. | 可以用滤纸来分离胶体和溶液 | D. | 胶体只能在液体中形成 |
8.下列关于 FeCl3水解的说法不正确的是( )
| A. | 水解达到平衡时(不饱和),加氯化铁溶液达饱和,溶液的酸性会增强 | |
| B. | 浓度为5 mol•L-1和0.5 mol•L-1的两种 FeCl3溶液,其他条件相同时,Fe3+的水解程度前者比后者小 | |
| C. | 有50℃和20℃的同浓度的两种FeCl3稀溶液,其他条件相同时,Fe3+的水解程度前者比后者小 | |
| D. | 为抑制 Fe3+的水解,较好地保存 FeCl3溶液,应加少量盐酸 |
15. 乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:
乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:
①25℃时有关弱酸的电离常数如表:
②Ksp(CaCO3)=2.8×10-9.
请回答下列问题:
(1)用pH试纸检测NaCN溶液的酸碱性时,pH试纸变为蓝色.用离子方程式解释出现这种现象的原因:CN-+H2O?HCN+OH-.
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液的pH=6,则$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$=$\frac{1}{18}$.
(3)在任一浓度的NaHCO3溶液中.c(OH-)-c(H+)=(填“>”、“=”或“<”)c(H2CO3)-c(CO32-).
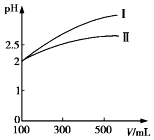
(4)体积均为100mL pH=2的CH3COOH溶液与HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶液的pH变化趋势的曲线是I(填“I”或“Ⅱ”).
(5)在容器中使氯化钙溶液与碳酸钠溶液等体积混合,己知碳酸钠溶液的浓度为2×l0-4mol/L,则生成沉淀所需氯化钙溶液的最小浓度为5.6×l0-5mol/L.
 乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:
乙酸、氰酸、碳酸等都是重要的碳的化合物.己知如下信息:①25℃时有关弱酸的电离常数如表:
| 弱酸的化学式 | CH3COOH | HCN | H2CO3 |
| 电离常数 | Ka=l.8×l0-5 | Ka=4.9×10-10 | Kal=4.3×10-7 Ka2=5.6×10-11 |
请回答下列问题:
(1)用pH试纸检测NaCN溶液的酸碱性时,pH试纸变为蓝色.用离子方程式解释出现这种现象的原因:CN-+H2O?HCN+OH-.
(2)25℃时,测得CH3COOH与CH3COONa的混合溶液的pH=6,则$\frac{c(C{H}_{3}COOH)}{c(C{H}_{3}CO{O}^{-})}$=$\frac{1}{18}$.
(3)在任一浓度的NaHCO3溶液中.c(OH-)-c(H+)=(填“>”、“=”或“<”)c(H2CO3)-c(CO32-).
(4)体积均为100mL pH=2的CH3COOH溶液与HCN溶液,加水稀释过程中溶液的pH变化与溶液体积的关系如图所示,则表示CH3COOH溶液的pH变化趋势的曲线是I(填“I”或“Ⅱ”).
(5)在容器中使氯化钙溶液与碳酸钠溶液等体积混合,己知碳酸钠溶液的浓度为2×l0-4mol/L,则生成沉淀所需氯化钙溶液的最小浓度为5.6×l0-5mol/L.
5.下列变化中,必须加入氧化剂才能发生的是( )
| A. | Na→Na2O2 | B. | SO2→S | C. | NaHCO3→CO2 | D. | HCl→H2 |
 .
.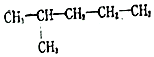 2-甲基戊烷
2-甲基戊烷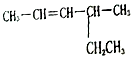 4-甲基-2-己烯.
4-甲基-2-己烯.