题目内容
9.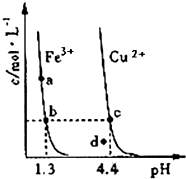 某温度下,将Fe(OH)3(s)、Cu(OH)2(s)分别置于蒸馏水中达到沉淀溶解平衡后,金属阳离子浓度随溶液pH的变化如图所示.下列判断正确的是( )
某温度下,将Fe(OH)3(s)、Cu(OH)2(s)分别置于蒸馏水中达到沉淀溶解平衡后,金属阳离子浓度随溶液pH的变化如图所示.下列判断正确的是( )| A. | 该温度下,Ksp[Fe(OH)3]>Ksp[Cu(OH)2] | |
| B. | c、d 两点代表的溶液中c(H+) 与c(OH-) 乘积不相等 | |
| C. | Cu(OH)2在c点比在d点代表的溶液中溶解程度小 | |
| D. | 加适量浓NH3•H2O可使溶液由a点变到b点 |
分析 A.根据图象找出可用来比较Fe(OH)3与Cu(OH)2溶度积常数点,可用b、c进行计算;
B.Kw只与温度有关,与溶液的酸碱性无关;
C.c点表示饱和溶液,在d点表示不饱和溶液;
D.由a点变到b点,pH增大.
解答 解:A.由b、c两点对应数据可比较出KSP[Fe(OH)3]与KSP[Cu(OH)2]的大小,KSP[Fe(OH)3]=c(Fe3+)•(OH-)3=c(Fe3+)•(10-12.7)3,KSP[Cu(OH)2]=c(Cu2+)•(OH-)2=c(Cu2+)•(10-9.6)2,因c(Fe3+)=c(Cu2+),故KSP[Fe(OH)3]<KSP[Cu(OH)2],故A错误;
B.只要温度不发生改变,溶液中c(H+)与c(OH-)的乘积(即Kw)就不变.该题中温度条件不变,故c、d两点代表的溶液中c(H+)与c(OH-)的乘积相等,故B错误;
C.在C点表示饱和溶液,在d点表示不饱和溶液,所以Cu(OH)2在c点比在d点代表的溶液中溶解程度大,故C错误;
D.向溶液中加入氨水,溶液的pH增大,则铁离子浓度降低,所以可以由a点变到b点,故D正确.
故选D.
点评 本题考查沉淀溶解平衡、溶度积、pH、水的离子积等知识点,为高频考点,侧重考查对图象中的数据进行定量或定性处理,找出数据(或坐标点)之间存在的相互关系;明确坐标点所表达的涵义;对溶度积和水的离子积有正确的理解.

练习册系列答案
相关题目
14.已知位于同周期的X、Y、Z三元素,它们的最高价氧化物的水化物分别为HXO4、H2YO4、H3ZO4,下列判断不正确的是( )
| A. | 阴离子的还原性:X<Y<Z | B. | 单质的氧化性:X>Y>Z | ||
| C. | 酸性:H3ZO4>H2YO4>HXO4 | D. | 气态氢化物的稳定性:X>Y>Z |
15.下列实验操作中错误的是( )
| A. | 用量筒量取12.12mL的盐酸 | |
| B. | 蒸馏时,应使温度计水银球靠近蒸馏烧瓶支管口 | |
| C. | 分液时,分液漏斗中下层液体从下口放出,上层液体从上口倒出 | |
| D. | 称量时,称量物应放在托盘天平的左盘,砝码放在托盘天平的右盘中 |
12.已知反应:
①2H2(g)+O2(g)═2H2O(g)△H1
②2H2(g)+O2(g)═2H2O(l)△H2
在相同条件下:2H2O(g)═2H2O(l)的焓变为( )
①2H2(g)+O2(g)═2H2O(g)△H1
②2H2(g)+O2(g)═2H2O(l)△H2
在相同条件下:2H2O(g)═2H2O(l)的焓变为( )
| A. | △H1-△H2 | B. | △H2-△H1 | C. | △H1+△H2 | D. | 2△H1-2△H2 |
4.利用工厂的废铁屑(含少量Fe2O3、SiO2、锡等),制备绿矾(FeSO4•7H2O)的过程如下:
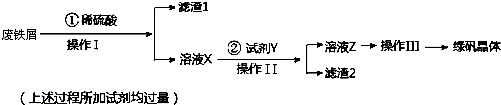
已知:①室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
②溶液X加KSCN不显红色.
(1)操作I的名称为过滤,所需玻璃仪器为烧杯、漏斗、玻璃棒.
(2)操作III的顺序依次为:加热蒸发、冷却结晶、过滤、洗涤、干燥.
(3)操作 II 中,试剂 Y 是H2S,然后用稀硫酸将溶液酸化至 pH=2 的目的是除去溶液中的Sn2+离子,并防止Fe2+离子生成沉淀.
(4)写出绿矾与酸性高锰酸钾溶液反应的离子方程式MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O.
(5)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至 pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失.
上述实验①②③所用氢氧化钠均不含杂质,且实验数据可靠.通过计算,分析和比较上表3组数据,给出结论.

已知:①室温下饱和H2S溶液的pH约为3.9,SnS沉淀完全时溶液的pH为1.6;FeS开始沉淀时溶液的pH为3.0,沉淀完全时的pH为5.5.
②溶液X加KSCN不显红色.
(1)操作I的名称为过滤,所需玻璃仪器为烧杯、漏斗、玻璃棒.
(2)操作III的顺序依次为:加热蒸发、冷却结晶、过滤、洗涤、干燥.
(3)操作 II 中,试剂 Y 是H2S,然后用稀硫酸将溶液酸化至 pH=2 的目的是除去溶液中的Sn2+离子,并防止Fe2+离子生成沉淀.
(4)写出绿矾与酸性高锰酸钾溶液反应的离子方程式MnO4-+5Fe2++8H+=5Fe3++Mn2++4H2O.
(5)常温下,称取不同氢氧化钠样品溶于水,加盐酸中和至 pH=7,然后将溶液蒸干得氯化钠晶体,蒸干过程中产品无损失.
| 氢氧化钠质量(g) | 氯化钠质量(g) | |
| ① | 2.40 | 3.51 |
| ② | 2.32 | 2.34 |
| ③ | 3.48 | 3.51 |
14.已知25℃时,电离常数Ka(HX)=3.6×10-4,溶度积常数Ksp(CaX2)=1.46×10-10.现向1L 0.2mol/LHX溶液中加入1L 0.2mol/LCaCl2溶液,则下列说法中正确的是( )
| A. | 25℃时,0.1 mol/LHX溶液中pH=1 | |
| B. | Ksp(CaX2)随温度和浓度的变化而变化 | |
| C. | 该体系中,c(Cl-)=c(Ca2+) | |
| D. | 该体系中HX与CaCl2反应产生沉淀 |
1.要使等浓度、等体积的AlCl3、CaCl2、NaCl溶液中的Cl-完全转化为AgCl沉淀,所用0.1mol•L-1AgNO3溶液的体积之比为( )
| A. | 1﹕2﹕3 | B. | 1﹕1﹕1 | C. | 2﹕3﹕6 | D. | 3﹕2﹕1 |
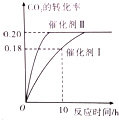 已知CO2可生成绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 300℃时密闭容器中,当c(CO2)=1.00mol/L、c(H2)=1.60mol/L开始反应,结果如图所示,回答下列问题:
已知CO2可生成绿色燃料甲醇.CO2(g)+3H2(g)?CH3OH(g)+H2O(g)△H<0 300℃时密闭容器中,当c(CO2)=1.00mol/L、c(H2)=1.60mol/L开始反应,结果如图所示,回答下列问题: