题目内容
20.化学与人类生活密切相关.关于下列物质的使用不合理的是( )| A. | 单质硅可用于制造光纤制品 | B. | 碳酸氢钠常用于焙制糕点 | ||
| C. | 氧化铝可用于制造耐火坩埚 | D. | 氢氧化铝常用于治疗胃酸过多 |
分析 A.二氧化硅是制造光纤制品;
B.碳酸氢钠不稳定,分解生成二氧化碳;
C.氧化铝的熔点高;
D.胃酸中含盐酸,可与氢氧化铝反应,降低酸性.
解答 解:A.二氧化硅是制造光纤制品,而不单质硅,单质是制半导体材料,故A错误;
B.碳酸氢钠不稳定,分解生成二氧化碳,则常用于焙制糕点,故B正确;
C.氧化铝的熔点高,所以可用于制造耐火坩埚,故C正确;
D.胃酸中含盐酸,可与氢氧化铝反应,降低酸性,且氢氧化铝的碱性较弱,则氢氧化铝常用于治疗胃酸过多,故D正确.
故选A.
点评 本题考查物质的性质,涉及二氧化硅、氧化铝、氢氧化铝、碳酸氢钠的化学性质,注意食品安全与物质性质的关系,题目难度不大.

练习册系列答案
 状元及第系列答案
状元及第系列答案 同步奥数系列答案
同步奥数系列答案
相关题目
10.根据以下三个热化学方程式:
2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H1
2H2S(g)+O2(g)═2S(s)+2H2O(l)△H2
2H2S(g)+O2(g)═2S(s)+2H2O(g)△H3
判断△H1、△H2、△H3三者关系正确的是( )
2H2S(g)+3O2(g)═2SO2(g)+2H2O(l)△H1
2H2S(g)+O2(g)═2S(s)+2H2O(l)△H2
2H2S(g)+O2(g)═2S(s)+2H2O(g)△H3
判断△H1、△H2、△H3三者关系正确的是( )
| A. | △H1>△H2>△H3 | B. | △H1>△H3>△H2 | C. | △H3>△H2>△H1 | D. | △H2>△H1>△H3 |
11.下列实验过程中,溶液中始终无明显现象的是( )
| A. | NO2通入FeSO4溶液中 | B. | CO2通入NaAlO2溶液中 | ||
| C. | Cl2通入NaOH溶液中 | D. | SO2通入Na2SiO3溶液中 |
5.13C-NMR(核磁共振)、15N-NMR可用于测定蛋白质、核酸等生物大分子的空间结构,KurtWü Thrich等人为此获得2002年诺贝尔化学奖.下面有关13C、15N叙述正确的是( )
| A. | 13C与15N有相同的质子数 | B. | 15N与14N是同种原子 | ||
| C. | 15N的核外电子数与中子数相同 | D. | 15N与14N互为同位素 |
12.“绿色化学”的主要内容之一是指从技术、经济上设计可行的化学反应,使原子充分利用,不产生污染物.下列化学反应符合“绿色化学”理念的是( )
| A. | 制CuSO4:Cu+2H2SO4(浓)═CuSO4+SO2↑+2H2O | |
| B. | 制Cu(NO3)2:Cu+4HNO3(浓)═Cu(NO3)2+2NO2↑+2H2O | |
| C. | 制CuSO4:2Cu+O2═2CuO; Cu+H2SO4(稀)═CuSO4+H2O | |
| D. | 制Cu(NO3)2:3Cu+8HNO3(稀)═3Cu(NO3)2+2NO↑+4H2O |
9.为了提纯下表所列物质(括号内为杂质),有关除杂试剂和分离方法的选择均正确的是( )
| 编号 | 被提纯的物质 | 除杂试剂 | 分离方法 |
| A | 乙烷(乙烯) | 酸性KMnO4溶液 | 分液 |
| B | 淀粉溶液(NaCl) | 水 | 过滤 |
| C | 苯(甲苯) | NaOH溶液 | 分液 |
| D | 甲烷(乙烯) | 溴水 | 洗气 |
| A. | A | B. | B | C. | C | D. | D |
10.下列物质所含粒子数或转移电子数为2NA(NA为阿伏加德罗常数的值)的是( )
| A. | 1molNa2O2所含的阴离子数 | |
| B. | 22.4LCO2所含氧原子数 | |
| C. | 2L1mol•L-1硫酸溶液中所含的氢离子数 | |
| D. | 点燃条件下,1molCl2与足量的钠充分反应时转移的电子数 |
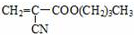 .其合成方法之一的路线如下:
.其合成方法之一的路线如下: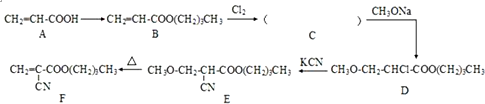
 .
.