题目内容
下列实验操作中,不能达到实验目的是( )
| A、溴乙烷与氢氧化钠溶液共煮后,加入硝酸银溶液检验Br- |
| B、用电石与饱和食盐水制乙炔 |
| C、用苯、浓硝酸和18.4mol/L的硫酸制硝基苯 |
| D、用稀硝酸洗涤做过银镜反应的试管 |
考点:化学实验方案的评价,乙炔炔烃,苯的性质,溴乙烷的化学性质
专题:有机物的化学性质及推断
分析:A.水解后显碱性,应在酸性条件显检验溴离子;
B.饱和食盐水与碳化钙生成乙炔,反应平稳;
C.苯与浓硝酸反应生成硝基苯,浓硫酸作催化剂、吸水剂;
D.Ag与稀硝酸反应.
B.饱和食盐水与碳化钙生成乙炔,反应平稳;
C.苯与浓硝酸反应生成硝基苯,浓硫酸作催化剂、吸水剂;
D.Ag与稀硝酸反应.
解答:
解:A.溴乙烷与氢氧化钠溶液共煮后,发生水解后显碱性,应加硝酸至酸性,再加入硝酸银溶液检验Br-,故A错误;
B.饱和食盐水与碳化钙生成乙炔,反应平稳,制备实验合理,故B正确;
C.苯与浓硝酸反应生成硝基苯,浓硫酸作催化剂、吸水剂,则用苯、浓硝酸和18.4mol/L的硫酸制硝基苯合理,故C正确;
D.Ag与稀硝酸反应,银镜反应后试管内壁的Ag可用稀硝酸清洗,故D正确;
故选A.
B.饱和食盐水与碳化钙生成乙炔,反应平稳,制备实验合理,故B正确;
C.苯与浓硝酸反应生成硝基苯,浓硫酸作催化剂、吸水剂,则用苯、浓硝酸和18.4mol/L的硫酸制硝基苯合理,故C正确;
D.Ag与稀硝酸反应,银镜反应后试管内壁的Ag可用稀硝酸清洗,故D正确;
故选A.
点评:本题考查化学实验方案的评价,为高频考点,涉及有机物水解实验及离子检验、有机物制备、仪器的洗涤等,侧重物质性质及实验原理的考查,注意实验方案非评价性、操作性分析,选项A为易错点,题目难度不大.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
有A、B、C、D、E五块金属片,进行如下实验:
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;
③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应;
⑤用惰性电极电解含B离子和E离子的溶液,E先析出.
据此,判断五种金属的活动性顺序是( )
①A、B用导线相连后,同时浸入稀H2SO4溶液中,A极为负极;
②C、D用导线相连后,同时浸入稀H2SO4溶液中,电流由D→导线→C;
③A、C相连后,同时浸入稀H2SO4溶液中,C极产生大量气泡;
④B、D相连后,同时浸入稀H2SO4溶液中,D极发生氧化反应;
⑤用惰性电极电解含B离子和E离子的溶液,E先析出.
据此,判断五种金属的活动性顺序是( )
| A、A>B>C>D>E |
| B、A>C>D>B>E |
| C、C>A>B>D>E |
| D、B>D>C>A>E |
下列除杂(括号内为杂质)有关操作,其中正确的是( )
| A、苯 (苯酚)--加入适量浓溴水,过滤 |
| B、NO (NO2)--通过水洗、干燥后,用向下排空气法收集 |
| C、乙烷 (乙烯)--让气体通过盛有酸性高锰酸钾溶液的洗气瓶 |
| D、乙醇 (乙酸)--加足量CaO固体,蒸馏 |
下列离子方程式正确的是( )
| A、铝与稀盐酸反应 Al+2H+=Al3++H2↑ |
| B、三氯化铁溶液与氢氧化钠溶液反应 FeCl3+3OH-=Fe(OH)3↓+3Cl- |
| C、用氢氧化钠溶液吸收多余的Cl2:Cl2+2OH-=Cl-+ClO-+H2O |
| D、二氧化碳与石灰水反应 CO2+2OH-=CO32-+H2O |
设NA为阿伏加德罗常数的值,下列说法正确的是( )
| A、常温下,1mol?L-1的NH4NO3溶液中含有氮原子的数目为2NA |
| B、常温下,100mL 1mol?L-1 AlCl3溶液中阳离子总数大于0.1NA |
| C、标准状况下,2.24L NO2含原子总数一定等于0.3NA |
| D、将2mol SO2与1mol O2混合,发生反应转移的电子总数一定是4NA |
下列说法正确的是( )
| A、同温同压下甲烷和氧气的密度之比为2:1 |
| B、1 g甲烷和1 g氧气的原子数之比为5:1 |
| C、等物质的量的甲烷和氧气的质量之比为2:1 |
| D、在标准状况下等质量的甲烷和氧气的体积之比为1:2 |
将1.12g铁粉加入25mL2mol/L的FeCl3溶液中,充分反应后,其结果是( )
| A、铁恰好将Fe3+全部还原 |
| B、往反应后溶液中滴入KSCN溶液,不显红色 |
| C、溶液变为浅绿色 |
| D、Fe2+和Fe3+物质的量之比为6:1 |
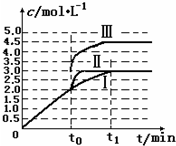 碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.
碳和氮是动植物体中的重要组成元素,向大气中过度排放二氧化碳会造成温室效应,氮氧化物会产生光化学烟雾,目前,这些有毒有害气体的处理成为科学研究的重要内容.