题目内容
13.原子序数大于4的主族元素A和B的离子Am+和Bn-它们的核外电子排布相同,据此推断:元素A和B所属周期序数之差为1;元素A和B的原子序数之差为m+n.分析 由Am+和Bn-它们的核外电子排布相同,则A在下一周期的前面,B在上一周期的后边,且ZA-m=ZB+n,则ZA-ZB=m+n,再由最高正价态来分析族,以此来解答.
解答 解:Am+和Bn-它们的核外电子排布相同,故A原子比B原子多一个电子层,故二者的周期数之差为1,
由核电荷数=原子序数=核外电子数,ZA-m=ZB+n,则ZA-ZB=m+n,
故答案为:1;m+n.
点评 本题考查位置、结构、性质,熟悉原子结构、核电荷数、原子序数、核外电子数的关系即可解答,明确核外电子排布相同是解答本题的关键,难度不大.

练习册系列答案
相关题目
3.有五种短周期元素,它们的结构、性质等信息如下表所述:
请根据表中信息填空:
(1)A原子的核外电子排布式为1s22s22p63s1.
(2)离子半径:B小于(填“大于”或“小于”)A.
(3)C原子的轨道表示式是 ,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
(4)D原子的电子排布式为1s22s22p63s23p5.
(5)C、E元素的第一电离能的大小关系是N>O(用元素符号表示).
| 元素 | 结构、性质等信息 |
| A | 是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,可用作制冷剂 |
| D | 是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
| E | L层上有2对成对电子 |
(1)A原子的核外电子排布式为1s22s22p63s1.
(2)离子半径:B小于(填“大于”或“小于”)A.
(3)C原子的轨道表示式是
 ,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.
,能量最高的电子为p轨道上的电子,其轨道呈哑铃形.(4)D原子的电子排布式为1s22s22p63s23p5.
(5)C、E元素的第一电离能的大小关系是N>O(用元素符号表示).
4.25℃时,下列有关溶液中微粒的物质的量浓度关系正确的是( )
| A. | 0.1 mol•L-1 CH3COONa溶液与0.1 mol•L-1 HCl溶液等体积混合:c(Na+)=c(Cl-)>c(CH3COO-)=c(OH-) | |
| B. | 0.1 mol•L-1NH4Cl溶液与0.1 mol•L-1氨水等体积混合(pH>7):c(NH3•H2O)>c(NH4+)>c(Cl-)>c(OH-) | |
| C. | 0.1 mol•L-1 Na2CO3溶液与0.1 mol•L-1 NaHCO3溶液等体积混合:$\frac{2}{3}$c(Na+)=c(CO32-)+c(HCO3-)+c(H2CO3) | |
| D. | 0.1 mol•L-1 Na2C2O4溶液与0.1 mol•L-1 HCl溶液等体积混合(H2C2O4为二元弱酸):2c(C2O42-)+c(HC2O4-)+c(OH-)=c(Na+)+c(H+) |
18.下列递变规律正确的是( )
| A. | Na、Mg、Al还原性依次增强 | B. | I2、Br2、Cl2氧化性依次减弱 | ||
| C. | C、N、O原子半径依次减小 | D. | P、S、F最高正价依次降低 |
5.石油减压分馏的目的是( )
| A. | 使高沸点的重油进一步分离 | B. | 分离得到汽油、煤油等轻质油 | ||
| C. | 得到高质量的汽油 | D. | 得到更多的优质重油 |
2.某有机物结构简式为  下列关于该有机物的说法中不正确的是( )
下列关于该有机物的说法中不正确的是( )
 下列关于该有机物的说法中不正确的是( )
下列关于该有机物的说法中不正确的是( )| A. | 遇FeCl 3溶液显紫色 | |
| B. | 1mol该有机物与足量的氢氧化溶液在一定条件下反应,最多消耗NaOH 3mol | |
| C. | 只能发生加成反应、取代反应和加聚反应 | |
| D. | 0.5mol该有机物与溴水发生加成反应,最多消耗0.5mol Br2. |
3.下列实验操作、现象、结论均正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 将溴乙烷与NaOH溶液共热后,滴加AgNO3溶液检测溴乙烷含Br原子 | 产生浅黄色沉淀 | 溴乙烷水解产生Br-离子与AgNO3溶液产生AgBr沉淀 |
| B | 向鸡蛋清水溶液中加CuSO4溶液 | 产生白色浑浊 | 蛋白质加盐,发生了盐析 |
| C | 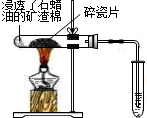 | 产生的气体会使KMnO4溶液褪色 | 石蜡油在碎瓷片作催化剂下裂解产生了不饱和烃 |
| D | 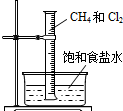 | 气体黄绿色变浅,量筒壁有油状液滴,液面上升 | 甲烷和氯气发生了氧化还原反应 |
| A. | A | B. | B | C. | C | D. | D |