题目内容
2.下列原子序数所代表的元素中,全属于主族元素的一组是( )| A. | 11 22 26 | B. | 13 15 38 | C. | 16 29 31 | D. | 18 21 31 |
分析 A.分别为Na、Ti、Fe;
B.分别为Al、P、Sr;
C.分别为S、Cu、Ga;
D.分别为Ar、Sc、Ga.
解答 解:A.分别为Na、Ti、Fe,只有Na为主族元素,故A不选;
B.分别为Al、P、Sr,均为主族元素,故B选;
C.分别为S、Cu、Ga,只有Cu为副族元素,故C不选;
D.分别为Ar、Sc、Ga,只有Ga为主族元素,故D不选;
故选B.
点评 本题考查元素周期表及应用,为高频考点,把握原子序数判断元素为解答的关键,侧重分析与应用能力的考查,注重基础知识的夯实与训练,题目难度不大.

练习册系列答案
 金钥匙试卷系列答案
金钥匙试卷系列答案
相关题目
12.下列过程属于吸热反应的是( )
| A. | 碘的升华 | B. | 铝粉与氧化铁粉末反应 | ||
| C. | 碳与二氧化碳反应生成一氧化碳 | D. | 镁与稀盐酸反应 |
13.如东海洋资源丰富,在开发利用海水资源过程中,下列说法不正确的是( )
| A. | 海水蒸发制海盐的过程是化学变化 | |
| B. | 海洋中有丰富的潮汐能、波浪能等新型能源 | |
| C. | 海水中提取溴单质的过程涉及氧化还原反应 | |
| D. | 海水淡化的方法主要有蒸馏法、离子交换法和电渗析发等 |
10.下列有关实验操作、现象和结论都正确的是( )
| 选项 | 实验操作 | 现象 | 结论 |
| A | 溶液中加入盐酸,再滴加BaCl2溶液 | 先无现象,后产生白色沉淀 | 原溶液中有SO42- |
| B | 向两份蛋白质溶液中分别滴加饱和Na2SO4溶液和CuSO4溶液 | 均有固体析出 | 蛋白质均发生变性 |
| C | 将Mg、Al与NaOH溶液组成原电池 | Mg电极溶解 | Mg比Al金属活动性强 |
| D | 向稀HNO3溶液中加入过量铁粉充分反应后,滴入KSCN溶液 | 溶液变为血红色 | 和HNO3具有氧化性,能将Fe氧化成Fe3+ |
| A. | A | B. | B | C. | C | D. | D |
17.关于元素周期表的说法正确的是( )
| A. | 目前元素周期表有7个周期 | B. | 元素周期表有8个主族 | ||
| C. | ⅢA族元素全部是金属元素 | D. | 非金属元素都在ⅣA~ⅤⅡA和0族 |
7.如图表示用酸性氢氧燃料电池为电源进行的电解实验.下列说法中正确的是( )
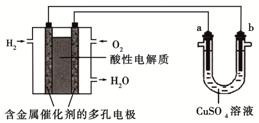

| A. | 燃料电池工作时,正极反应为:O2+2H2O+4e-═4OH- | |
| B. | a极是铁,b极是铜时,b极逐渐溶解,a极上有铜析出 | |
| C. | a极是粗铜,b极是纯铜时,a极逐渐溶解,b极上有铜析出 | |
| D. | a、b两极均是石墨时,a极上产生的O2与电池中消耗的H2的体积比为2:1 |
14.下列化合物中存在离子键的是( )
| A. | 氯化氢 | B. | 甲烷 | C. | 水 | D. | 硫化钠 |
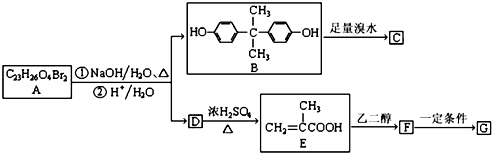
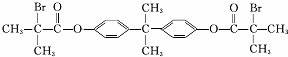
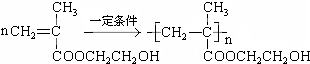 .
.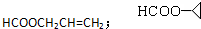 .
.