题目内容
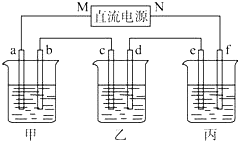 如图所示装置中,甲、乙、丙三个烧杯依次分别盛放NaCl溶液、足量的AgNO3溶液和 K2SO4溶液,电极均为石墨电极.
如图所示装置中,甲、乙、丙三个烧杯依次分别盛放NaCl溶液、足量的AgNO3溶液和 K2SO4溶液,电极均为石墨电极.(1)接通电源,经过一段时间后,测得a电极产生标准状况下的气体2.24L,c电极质量增加.据此回答问题:
①电源的N端为
②电极c质量变化是
③电极f上生成的气体在标准状况下的体积
④电解前后各溶液的pH值的变化(填“不变”、“变大”或“变小”)甲溶液
(2)如果电解过程中银全部析出,此时电解能否继续进行,为什么?
考点:电解原理
专题:电化学专题
分析:(1)①乙中C电极质量增加,则c处发生的反应为:Ag++e-=Ag,即C处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极,f为阳极,e为阴极,d为阳极,甲池是电解饱和氯化钠溶液;
②依据电极反应电子守恒计算,乙中为AgNO3溶液,c为阴极电极反应Ag++e-=Ag,d电极为阳极,氢氧根离子失电子发生氧化反应;
③丙中为K2SO4,相当于电解水,f电极生成的是氧气,整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的,依据电子守恒和电极反应计算f电极生成氧气的体积;
④甲中电解氯化钠溶液是电解水和氯化钠,溶液中生成NaOH的浓度增大,pH变大.乙中阴极为Ag+放电,阳极为OH-放电,所以H+增多,故pH减小.丙中为电解水,对于K2SO4而言,其pH几乎不变;
(2)银全部析出,可以继续电解H2SO4,有电解液即可电解.
②依据电极反应电子守恒计算,乙中为AgNO3溶液,c为阴极电极反应Ag++e-=Ag,d电极为阳极,氢氧根离子失电子发生氧化反应;
③丙中为K2SO4,相当于电解水,f电极生成的是氧气,整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的,依据电子守恒和电极反应计算f电极生成氧气的体积;
④甲中电解氯化钠溶液是电解水和氯化钠,溶液中生成NaOH的浓度增大,pH变大.乙中阴极为Ag+放电,阳极为OH-放电,所以H+增多,故pH减小.丙中为电解水,对于K2SO4而言,其pH几乎不变;
(2)银全部析出,可以继续电解H2SO4,有电解液即可电解.
解答:
解:(1)接通电源,经过一段时间后,测得a电极产生标准状况下的气体2.24L,物质的量为0.1mol,c电极质量增加,则c处发生的反应为:Ag++e-=Ag,即C处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极,f为阳极,e为阴极,d为阳极;
①乙中C电极质量增加,则c处发生的反应为:Ag++e-=Ag,即C处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极,f为阳极,e为阴极,d为阳极,甲池是电解饱和氯化钠溶液,电解反应的离子方程式为:2Cl-+2H2O
Cl2↑+H2↑+2OH-;
故答案为:正,2Cl-+2H2O
Cl2↑+H2↑+2OH-;
②依据电极反应电子守恒计算,a电极产生标准状况下的气体2.24L,物质的量为0.1mol,电极反应为:2H++2e-=H2↑,电子转移0.2mol;乙中为AgNO3溶液,c为阴极电极反应Ag++e-=Ag,依据电子守恒,c电极质量增加银物质的量0.2mol,质量=0.2mol×108g/mol=21.6g;d电极为阳极,氢氧根离子失电子发生氧化反应,电极反应4OH--4e-=O2↑+2H2O;
故答案为:21.6,4OH--4e-=O2↑+2H2O;
③丙中为K2SO4,相当于电解水,f电极生成的是氧气,整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的,依据电子守恒和电极反应计算f电极生成氧气的体积,根据电解反应计算,4OH--4e-=O2↑+2H2O,生成氧气体积标准状况0.05mol×22.4L/mol=0.112L;
故答案为:0.112L;
④甲中电解氯化钠溶液是电解水和氯化钠,溶液中生成NaOH的浓度增大,pH变大.乙中阴极为Ag+放电,阳极为OH-放电,所以H+增多,故pH减小.丙中为电解水,对于K2SO4而言,其pH几乎不变;
故答案为:变大、减小,不变;
(2)银全部析出,可以继续电解稀硝酸,有电解液即可电解;
故答案为:能,若Ag全部析出,溶液为稀硝酸,电解仍然继续进行.
①乙中C电极质量增加,则c处发生的反应为:Ag++e-=Ag,即C处为阴极,由此可推出b为阳极,a为阴极,M为负极,N为正极,f为阳极,e为阴极,d为阳极,甲池是电解饱和氯化钠溶液,电解反应的离子方程式为:2Cl-+2H2O
| ||
故答案为:正,2Cl-+2H2O
| ||
②依据电极反应电子守恒计算,a电极产生标准状况下的气体2.24L,物质的量为0.1mol,电极反应为:2H++2e-=H2↑,电子转移0.2mol;乙中为AgNO3溶液,c为阴极电极反应Ag++e-=Ag,依据电子守恒,c电极质量增加银物质的量0.2mol,质量=0.2mol×108g/mol=21.6g;d电极为阳极,氢氧根离子失电子发生氧化反应,电极反应4OH--4e-=O2↑+2H2O;
故答案为:21.6,4OH--4e-=O2↑+2H2O;
③丙中为K2SO4,相当于电解水,f电极生成的是氧气,整个电路是串联的,故每个烧杯中的电极上转移电子数是相等的,依据电子守恒和电极反应计算f电极生成氧气的体积,根据电解反应计算,4OH--4e-=O2↑+2H2O,生成氧气体积标准状况0.05mol×22.4L/mol=0.112L;
故答案为:0.112L;
④甲中电解氯化钠溶液是电解水和氯化钠,溶液中生成NaOH的浓度增大,pH变大.乙中阴极为Ag+放电,阳极为OH-放电,所以H+增多,故pH减小.丙中为电解水,对于K2SO4而言,其pH几乎不变;
故答案为:变大、减小,不变;
(2)银全部析出,可以继续电解稀硝酸,有电解液即可电解;
故答案为:能,若Ag全部析出,溶液为稀硝酸,电解仍然继续进行.
点评:本题为电化学知识的综合应用,做题时要注意根据电极反应现象判断出电解池的阴阳级,进而判断出电源的正负极,要注意三个电解池为串联电路,各电极上得失电子的数目相等.做题时要正确写出电极方程式,准确判断两极上离子的放电顺序.

练习册系列答案
相关题目
在四个相同的容器中,不同的温度下(其他条件相同)进行合成R:[P(g)+3Q(g)?2R(g)△H<0的反应,根据下列在未达到平衡时的相同时间内测得的结果判断,达到平衡时Q的转化率最高的是( )
| A、v(R)=0.1mol?L-1?min-1 |
| B、v(P)=0.3mol?L-1?min-1 |
| C、v(Q)=0.3mol?L-1?min-1 |
| D、v(Q)=0.6mol?L-1?min-1 |
下列物质:①盐酸 ②NaOH ③AlCl3 ④明矾 ⑤硫酸铝 ⑥碱式氯化铝 ⑦生石灰.能在水处理中作混凝剂的是( )
| A、①④⑤⑥ | B、②③④⑤ |
| C、③④⑤⑥ | D、全部 |
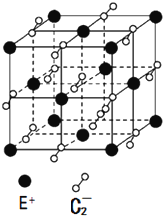 A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次递增.已知B、D两种元素原子的最外层电子数是最内层电子数的两倍,而C元素原子的最外层电子数等于B元素原子的核外电子数,E的价电子数为1.回答下列问题.
A、B、C、D、E都是元素周期表中的前20号元素,它们的原子序数依次递增.已知B、D两种元素原子的最外层电子数是最内层电子数的两倍,而C元素原子的最外层电子数等于B元素原子的核外电子数,E的价电子数为1.回答下列问题.