题目内容
10.核内中子数为N的R2+离子,质量数为A,则ng它的氧化物中所含质子的物质的是( )| A. | $\frac{n}{16+A}$(A-N+8)mol | B. | $\frac{n}{16+A}$(A-N+10)mol | C. | (A-N+2)mol | D. | $\frac{n}{A}$(A-N+6)mol |
分析 核内中子数为N的R2+离子,质量数为A,所以质子数为A-N,该离子的相对原子质量在数值上等于其质量数;该离子带2个单位正电荷,所以其氧化物的化学式为RO;该氧化物的摩尔质量为(A+16)g/mol,一个氧化物分子中含有(A-N+8)个质子.
解答 解:该氧化物的摩尔质量为(A+16)g/mol,n g 它的氧化物的物质的量为$\frac{ng}{(A+16)g/mol}$;
一个氧化物分子中含有(A-N+8)个质子,所以ng 它的氧化物中所含质子的物质的量为$\frac{ng}{(A+16)g/mol}$×(A-N+8)=$\frac{n(A-N+8)}{(A+16)}$,
故选:A.
点评 本题考查了质子数、中子数、质量数之间的关系,明确原子的相对原子质量等于其质量数是解题关键,题目难度不大.

练习册系列答案
 中考解读考点精练系列答案
中考解读考点精练系列答案
相关题目
18.下列化学用语正确的是( )
| A. | 乙烯的结构简式可表示为CH2CH2 | B. | 乙醇的分子式:CH3CH2OH | ||
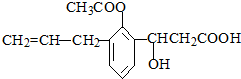
| C. | 甲烷的结构式:CH4 | D. | 甲苯的键线式可表示为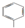 |
15.某有机物的结构简式如图,有关说法正确的是( )

| A. | 该物质共有两种含氧官能团 | |
| B. | 该物质属于芳香烃 | |
| C. | 1 mol该有机物能与3mol的NaOH反应 | |
| D. | 1 mol该有机物在一定条件下可以消耗6molH2 |
2.下列有关元素周期表的说法正确的是( )
| A. | 第I A族元素都是碱金属元素 | |
| B. | 元素周期表中有18个纵行,所以有18个族 | |
| C. | 可以从过渡金属中寻找新型催化剂 | |
| D. | 主族元素的金属元素原子最外层电子数一定小于或等于4 |
20.下列反应属于吸热反应的是( )
| A. | 碳酸钙受热分解 | B. | 乙醇燃烧 | C. | 炸药爆炸 | D. | 氧化钙溶于水 |

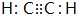 ;D的最简式CH2;
;D的最简式CH2; +Br2 $\stackrel{FeBr_{3}}{→}$
+Br2 $\stackrel{FeBr_{3}}{→}$ +HBr,其反应类型为取代反应.
+HBr,其反应类型为取代反应.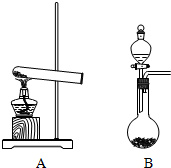 如图,实验室制取氨气有几种方法,
如图,实验室制取氨气有几种方法,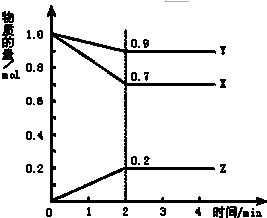 某温度时,在2L容器中X、Y、Z三种物质随时间的变化曲线如图所示,由图中的数据分析,反应开始至2min时:
某温度时,在2L容器中X、Y、Z三种物质随时间的变化曲线如图所示,由图中的数据分析,反应开始至2min时: