题目内容
16.下列对应关系不正确的是( )| 选项 | A | B | C | D |
| 中心原子所在族 | ⅣA族 | ⅤA族 | ⅣA族 | ⅥA族 |
| 分子通式 | AB4 | AB3 | AB2 | AB2 |
| 立体构型 | 正四面体形 | 平面三角形 | 直线形 | V形 |
| A. | A | B. | B | C. | C | D. | D |
分析 对于ABn型分子,中心原子A的价层电子对数=n+孤电子对数,根据孤电子对数、价层电子对数确定空间构型,而孤电子对数=$\frac{1}{2}$(a-xb),a为中心原子的价电子数,x为中心原子结合的原子数,b为与中心原子结合的原子最多接受的电子数,氢为1,其它原子等于“8-该原子价电子数”.
解答 解:A.中心原子处于ⅣA族,分子组成通式为AB4,A原子最外层4个电子全部成键,孤电子对数为0,价层电子对数为4,故空间构型为正四面体,故A正确;
B.中心原子处于VA族,分子组成通式为AB3,A原子最外层3个电子成键,孤电子对数为1,价层电子对数为4,故空间构型为三角锥形,故B错误;
C.中心原子处于ⅣA族,分子组成通式为AB2,A原子最外层4个电子全部成键,孤电子对数为0,价层电子对数为2,故空间构型为直线型,故C正确;
D.中心原子处于ⅥA族,分子组成通式为AB2,A原子最外层6个电子没有全部成键,存在孤电子对数,故空间构型为V形,故D正确,
故选:B.
点评 本题考查微粒空间构型判断,掌握价层电子对互斥理论,理解VSEPR模型与立体构型.

练习册系列答案
 学而优暑期衔接南京大学出版社系列答案
学而优暑期衔接南京大学出版社系列答案 Happy holiday欢乐假期暑假作业广东人民出版社系列答案
Happy holiday欢乐假期暑假作业广东人民出版社系列答案
相关题目
6.下列实验装置进行相应的实验,不能达到实验目的是( )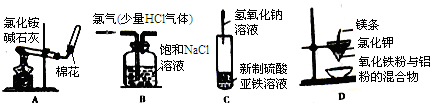

| A. | 实验室制取并收集氨气 | B. | 除去Cl2中的HCl气体杂质 | ||
| C. | 实验室制取氢氧化亚铁 | D. | 铝热反应实验 |
7.中学化学常见物质存在转化关系:A+B→C+D+H2O,其中C属于盐类,下列推断不正确的是( )
| A. | 若A为黄绿色气体,则D可能有漂白性 | |
| B. | 若A为红色金属单质,则D一定是红棕色气体 | |
| C. | 若A为纯碱,则D一定能使澄清石灰水变浑浊 | |
| D. | 若A为氯化铵,则D一定是具有刺激性气味的气体 |
4.能正确表示下列反应的离子方程式为( )
| A. | 向FeI2溶液中滴入过量溴水:2Fe2++2I-+2Br2═2Fe3++I2+4Br- | |
| B. | 将Na2O2放入H2O中:2Na2O2+2H2O═4Na++4OH-+H2↑ | |
| C. | 向NaHSO4溶液中滴入少量Ba(OH)2溶液:H++SO42-+Ba2++OH-═BaSO4↓+H2O | |
| D. | 将稀盐酸与84消毒液混合:C1-+C1O-+2H+═C12↑+H2O |
11.关于下列四幅图中相应实验的说法错误的是( )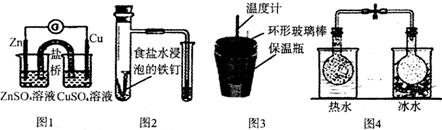

| A. | 图1中根据电流计(G)指针的偏转方向可比较Zn2+、Cu2+的氧化性强弱 | |
| B. | 图2中根据导气管中液面的变化可以判断铁钉发生了吸氧腐蚀 | |
| C. | 图3中若改用环形铜棒不会影响所测中和热的数值 | |
| D. | 图4中发生反应2NO2(g)?N2O4(g),根据两烧瓶中气体颜色深浅不同可判断其为放热反应 |
7.进行化学实验必须注意安全,下列说法不正确的是( )
| A. | 不慎将少量酸溅到眼中,应立即用水洗,边洗边眨眼睛 | |
| B. | 不慎将浓碱溶液沾到皮肤上,要立即用大量水冲洗,然后涂上硼酸溶液 | |
| C. | 配制稀硫酸时,可先在量筒中加入一定体积的水,再在搅拌下慢慢加入浓硫酸 | |
| D. | 酒精着火时,可用湿抹布将其扑灭 |

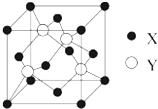 元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.
元素X位于第四周期,其基态原子的内层轨道全部排满电子,且最外层电子数为2.元素Y基态原子的3p轨道上有4个电子.元素Z的原子最外层电子数是其内层的3倍.