��Ŀ����
 2SO3(g)����H= -QkJ/mol�������������·ֱ���������ͷ�Ӧ�ų�������(Q)���±����С��ж�����������ȷ����
2SO3(g)����H= -QkJ/mol�������������·ֱ���������ͷ�Ӧ�ų�������(Q)���±����С��ж�����������ȷ���� 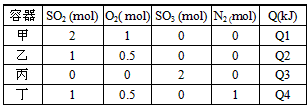
B��ƽ��ʱ�����߱������¶ȣ�����Ӧ���������淴Ӧ���ʼ�С��ƽ�������ƶ�
C���������з�Ӧ�ų������Ĺ�ϵΪ��Q1=2Q2>2Q4
D���������з�Ӧ�ﵽƽ��ʱ���仯ѧƽ�ⳣ��С���������з�Ӧ��ƽ�ⳣ��

 ��ɢ˼ά�¿���ϵ�д�
��ɢ˼ά�¿���ϵ�д������仯�����ڹ�ũҵ������������������Ҫ���á���ش��������⣺
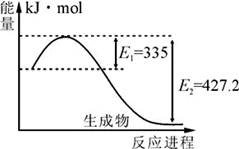
��1����ͼ��N2��H2��Ӧ����2molNH3�����������仯ʾ��ͼ��ÿ����1molNH3�ų�����Ϊ ��
��2�������Ϊ2L���ܱ������У��������»�ѧ��Ӧ��
N2��g����3H2��g��2NH3��g�� ��H��0���õ��������ݣ�
| ʵ���� | �¶ȡ� | ��ʼ��/mol | 2����/mol | ƽ�ⳣ�� | |
| H2 | N2 | NH3 | |||
| 1 | 298 | 6 | 2 | 1.2 | 4.1��106 |
| 2 | 398 | 3 | 1 | 0.8 | K1 |
��ش��������⣺
�� K1����Դ�С��K1_______4.1��106����д��������������������
��ʵ��1���Ԧ�(H2) ��ʾ�ķ�Ӧ����Ϊ ��
�����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�����ݵ��� ���������ĸ����
A.������N2��H2��NH3�����ʵ���Ũ��֮��Ϊ1��3��2
B.�ԣ�N2�������� ��3�ԣ�H2�����棩
C.������ѹǿ���ֲ���
D.���������ܶȱ��ֲ���
(3)��һ�������ºϳɰ���Ӧ��ƽ����ں��������³��뺤��������Ӧ���� ���������С�������䡱���ں�ѹ�����£����뺤����ƽ�� �ƶ�������������������
��4�� NH4Cl��Һ�����ԣ���������NH4��ˮ���Ե�ʡ���NH4Cl����ˮ��D2O����ˮ������ӷ���ʽ�� ��
�����仯�����ڹ�ũҵ������������������Ҫ���á���ش��������⣺
��1����ͼ��N2��H2��Ӧ����2molNH3�����������仯ʾ��ͼ��ÿ����1molNH3�ų�����Ϊ ��
��2�������Ϊ2L���ܱ������У��������»�ѧ��Ӧ��
N2��g����3H2��g�� 2NH3��g��
��H��0���õ��������ݣ�
2NH3��g��
��H��0���õ��������ݣ�
|
ʵ���� |
�¶ȡ� |
��ʼ��/mol |
2����/mol |
ƽ�ⳣ�� |
|
|
H2 |
N2 |
NH3 |
|||
|
1 |
298 |
6 |
2 |
1.2 |
4.1��106 |
|
2 |
398 |
3 |
1 |
0.8 |
K1 |
��ش��������⣺
�� K1����Դ�С��K1_______4.1��106����д��������������������
��ʵ��1���Ԧ�(H2) ��ʾ�ķ�Ӧ����Ϊ ��
�����и�������Ϊ�жϸ÷�Ӧ�ﵽ��ѧƽ��״̬�����ݵ��� ���������ĸ����
A.������N2��H2��NH3�����ʵ���Ũ��֮��Ϊ1��3��2
B.�ԣ�N2�������� ��3�ԣ�H2�����棩
C.������ѹǿ���ֲ���
D.���������ܶȱ��ֲ���
(3)��һ�������ºϳɰ���Ӧ��ƽ����ں��������³��뺤��������Ӧ���� ���������С�������䡱���ں�ѹ�����£����뺤����ƽ�� �ƶ�������������������
��4�� NH4Cl��Һ�����ԣ���������NH4��ˮ���Ե�ʡ���NH4Cl����ˮ��D2O����ˮ������ӷ���ʽ�� ��