题目内容
C、N、S都是重要的非金属元素.下列说法正确的是( )
| A、三者对应的氧化物均为酸性氧化物 |
| B、实验室可用NaOH溶液处理SO2、NO2 |
| C、CO2、NO2、SO2都能与H2O反应,其反应原理相同 |
| D、三者的单质直接与氧气反应都能生成两种氧化物 |
考点:酸、碱、盐、氧化物的概念及其相互联系,二氧化硫的污染及治理,碳族元素简介
专题:
分析:A.CO、NO为不成盐氧化物;
B.SO2、NO2都有毒,且都可以和NaOH溶液反应;
C.二氧化氮和水反应属于氧化还原反应;
D.氮气和氧气反应生成NO,硫在氧气中燃烧生成二氧化硫.
B.SO2、NO2都有毒,且都可以和NaOH溶液反应;
C.二氧化氮和水反应属于氧化还原反应;
D.氮气和氧气反应生成NO,硫在氧气中燃烧生成二氧化硫.
解答:
解:A.CO、NO为不成盐氧化物,所以三者对应的氧化物不均为酸性氧化物,故A错误;
B.SO2+2NaOH=Na2SO3+H2O、3NO2+2NaOH=2NaNO3+NO+H2O,故B正确;
C.CO2+H2O=H2CO3、SO2+H2O=H2SO3中没有电子转移属于非氧化还原反应,3NO2+H2O=2HNO3+NO中有电子转移属于氧化还原反应,故C错误;
D.氮气和氧气反应生成NO,NO被氧气氧化生成二氧化氮,S在氧气中燃烧生成二氧化硫,故D错误;
故选B.
B.SO2+2NaOH=Na2SO3+H2O、3NO2+2NaOH=2NaNO3+NO+H2O,故B正确;
C.CO2+H2O=H2CO3、SO2+H2O=H2SO3中没有电子转移属于非氧化还原反应,3NO2+H2O=2HNO3+NO中有电子转移属于氧化还原反应,故C错误;
D.氮气和氧气反应生成NO,NO被氧气氧化生成二氧化氮,S在氧气中燃烧生成二氧化硫,故D错误;
故选B.
点评:本题考查非金属元素及其化合物的性质,涉及尾气处理、氧化还原反应的判断等知识点,熟练掌握C、N、S、Cl元素及其化合物性质并灵活运用,为高考高频点,题目难度不大.

练习册系列答案
 新课标快乐提优暑假作业陕西旅游出版社系列答案
新课标快乐提优暑假作业陕西旅游出版社系列答案 暑假衔接培优教材浙江工商大学出版社系列答案
暑假衔接培优教材浙江工商大学出版社系列答案
相关题目
同温同压下,等质量的SO2和CO2相比较,下列叙述中正确的是( )
| A、电子数之比1:1 |
| B、体积比16:11 |
| C、密度比16:11 |
| D、氧原子数之比为1:1 |
下列反应的离子方程式正确的是( )
| A、氢氧化钡中加入稀硫酸:Ba2++OH-+SO42-+H+=BaSO4↓+H2O |
| B、氧化铜溶于稀硫酸:2H++CuO=Cu2++H2O |
| C、碳酸钙溶于盐酸:CO32-+2H+=CO2↑+H2O |
| D、铁与氯化铁溶液反应:Fe+Fe3+=2Fe2+ |
下列离子方程式书写正确的是( )
| A、向稀硫酸中加入氢氧化钡溶液 H++SO42-+Ba2++HO-=H2O+BaSO4↓ |
| B、向石灰水中加入硝酸溶液 H++OH-=H2O |
| C、向氧化镁中加入硫酸溶液 Mg2++SO42-=MgSO4 |
| D、向硝酸银溶液中加入锌粉 Zn+Ag+=Zn2++Ag |
经测定:常温、常压下的一瓶气体中只含有C、O两种元素,通常情况下,这瓶气体不可能是( )
| A、一种纯净的化合物 |
| B、一种单质和一种化合物的混合物 |
| C、两种化合物的混合物 |
| D、两种单质的混合物 |
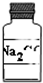 固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )
固体A的试剂瓶签已部分被腐蚀(如图所示).已知固体A只可能是Na2CO3、Na2SO3和Na2SO4中的一种.若取少量固体A配成稀溶液进行实验鉴定,下列说法错误的是( )| A、只用盐酸一种试剂就可以确定该固体A的成分 |
| B、依次加入Ba(NO3)2溶液、盐酸,若有白色沉淀,则固体A为Na2SO4 |
| C、滴入酸性KMnO4溶液,若KMnO4溶液褪色,则固体A为Na2SO3 |
| D、用pH试纸检验(常温),若pH>7,则固体A可能是Na2CO3 |