题目内容
19.填写下列空白:(1)写出表示含有8个质子、10个中子的原子的化学符号:188O;
(2)周期表中最活泼的非金属元素位于第ⅦA族;
(3)所含元素种类是8种的周期是第二、三周期.
(4)氯元素在周期表中位于第三周期第ⅦA族.氯的最高价氧化物的化学式为Cl2O7,最高价氧化物的水化物的化学式为HClO4.
分析 (1)质子数为8的原子为氧原子,利用质量数=质子数+中子数来分析;
(2)非金属强的元素在元素周期表中的右上方的位置;
(3)所含元素种类是8种的周期在短周期,短周期包括一、二、三周期;
(4)氯元素在周期表中位于第三周期,第ⅦA族,最高价是+7价,所以氧化物为:Cl2O7,最高价氧化物的水化物的化学式为HClO4.
解答 解:(1)质子数为8的原子为氧原子,则含8个质子、10个中子的原子的质量数=8+10=18,化学符号为188O,
故答案为:188O;
(2)非金属强的元素在元素周期表中的右上方的位置,在每个周期中第ⅦA族元素的非金属性最强,在第ⅦA族中Cl元素的非金属性最强,故答案为:ⅦA;
(3)短周期包括一、二、三周期,第一周期有2种元素,第二、三周期都含有8种元素,故答案为:二;三;
(4)氯元素在周期表中位于第三周期,第ⅦA族,最高价是+7价,所以氧化物为:Cl2O7,最高价氧化物的水化物的化学式为HClO4,故答案为:三;ⅦA;Cl2O7;HClO4.
点评 本题考查原子的构成及元素在周期表中的位置和性质,注重基础,难度不大,明确元素周期表的结构是解答本题的关键.

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目
9.反应A(g)+3B(g)?2C(g)+2D(g)分别从下列两条途径建立平衡:Ⅰ.A、B的起始物质的量分别为2mol和6mol;Ⅱ.C、D的起始物质的量均为2mol.在温度、压强恒定的条件下,以下叙述中不正确的是( )
| A. | Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的百分组成相同 | |
| B. | 达平衡时,途径Ⅰ所得混合气体的密度为途径Ⅱ所得混合气体密度的$\frac{1}{2}$ | |
| C. | 达平衡时,途径Ⅰ的反应速率v(A)等于途径Ⅱ的反应速率v(A) | |
| D. | Ⅰ、Ⅱ两途径最终达到平衡时,体系内混合气体的平均相对分子质量相同 |
10.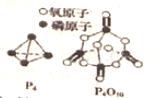 已知1mol白磷(P4)完全燃烧放热为dkJ,白磷及其完全燃烧的产物结构如图所示,下表是部分化学键的键能数据,则表中x(用含有a、b、c、d的代数式表示)为( )
已知1mol白磷(P4)完全燃烧放热为dkJ,白磷及其完全燃烧的产物结构如图所示,下表是部分化学键的键能数据,则表中x(用含有a、b、c、d的代数式表示)为( )
 已知1mol白磷(P4)完全燃烧放热为dkJ,白磷及其完全燃烧的产物结构如图所示,下表是部分化学键的键能数据,则表中x(用含有a、b、c、d的代数式表示)为( )
已知1mol白磷(P4)完全燃烧放热为dkJ,白磷及其完全燃烧的产物结构如图所示,下表是部分化学键的键能数据,则表中x(用含有a、b、c、d的代数式表示)为( ) | 化学键 | P-P | P-O | O=O | P=O |
| 键能/kJ•mol-1 | a | b | c | x |
| A. | 12b-d-6a-5c | B. | -(d+6a+5c-12b) | C. | d+6a+5c-12b | D. | d+6a.5c-12b |
7.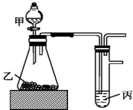 用如图装置进行实验,根据实验现象所得结论正确的是( )
用如图装置进行实验,根据实验现象所得结论正确的是( )
 用如图装置进行实验,根据实验现象所得结论正确的是( )
用如图装置进行实验,根据实验现象所得结论正确的是( )| 甲 | 乙 | 丙 | 结论 | |
| A | 盐酸 | 石灰石 | 漂白粉溶液 | 酸性:HCl>H2CO3>HClO |
| B | 盐酸 | 硫化亚铁 | 硫酸铜溶液 | 酸性:HCl>H2S>H2SO4 |
| C | 水 | 过氧化钠 | 水 | 过氧化钠与水的反应是放热反应 |
| D | 浓盐酸 | 二氧化锰 | 碘化钾溶液 | 氧化性:MnO2>Cl2>I2 |
| A. | A | B. | B | C. | C | D. | D |
4.化学与能源开发、环境保护、资源利用等密切相关.下列说法正确的是( )
| A. | “无磷洗涤剂”的推广使用,不能有效减少水体富营养化的发生 | |
| B. | 无论是风力发电还是火力发电,都是将化学能转化为电能 | |
| C. | PM2.5含有的铅、镉、铬、钒、砷等对人体有害的元素均是金属元素 | |
| D. | 硫的氧化物和氮的氧化物是形成酸雨的主要物质 |
11.下列关于糖类、油脂、蛋白质的说法不正确的是( )
| A. | 蛋白质、纤维素、蔗糖、油脂都是高分子化合物 | |
| B. | 可用浓硝酸鉴别含苯环的蛋白质 | |
| C. | 工业上利用油脂在碱的催化作用下水解生产肥皂 | |
| D. | 淀粉水解与纤维素水解得到的最终产物相同 |
8.苯和乙炔相比较,下列叙述不正确的是( )
| A. | 都能发生燃烧,生成二氧化碳和水 | |
| B. | 乙炔易发生加成反应,苯只能在特殊条件下才能发生加成反应 | |
| C. | 都能被KMnO4氧化,使高锰酸钾酸性溶液褪色 | |
| D. | 相同质量的苯和乙炔,完全燃烧时耗氧量相同 |
9.下列物质属于酸性氧化物的是( )
| A. | CO | B. | K2SO4 | C. | SO2 | D. | Na20 |

 .
.