题目内容
6.下列反应的离子方程式正确的是( )| A. | 向Al2(SO4)3溶液中逐滴滴入Ba(OH)2溶液至SO42-恰好沉淀完全:2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓ | |
| B. | 用惰性电极电解熔融氯化钠:2Cl-+2H2O$\frac{\underline{\;通电\;}}{\;}$Cl2↑+H2↑+2OH- | |
| C. | 硫化钠发生水解:S2-+2H2O═H2S+2OH- | |
| D. | 向NH4HSO4溶液中加入NaOH溶液至混合液呈中性:H++OH-═H2O |
分析 A.至SO42-恰好沉淀完全,生成硫酸钡和氢氧化铝;
B.惰性电极电解熔融氯化钠,生成Na和氯气;
C.水解为可逆反应,且硫离子水解以第一步为主;
D.溶液呈中性,NH4HSO4、NaOH的物质的量大于1:1,小于2:1,则溶液中存在硫酸钠、硫酸铵以及一水合氨.
解答 解:A.向Al2(SO4)3溶液中逐滴滴入Ba(OH)2溶液至SO42-恰好沉淀完全的离子反应为2Al3++3SO42-+3Ba2++6OH-═3BaSO4↓+2Al(OH)3↓,故A正确;
B.用惰性电极电解熔融氯化钠的反应为2Cl-+2Na+$\frac{\underline{\;通电\;}}{\;}$Cl2↑+2Na,故B错误;
C.硫化钠发生水解离子反应为S2-+H2O?HS-+OH-,故C错误;
D.向NH4HSO4溶液中加入NaOH溶液至混合液呈中性时存在H++OH-═H2O、NH4++OH-═NH3.H2O,NH4HSO4、NaOH的物质的量大于1:1,小于2:1,故D错误;
故选A.
点评 本题考查离子反应方程式书写的正误判断,为高频考点,把握发生的反应及离子反应的书写方法为解答的关键,侧重复分解反应、水解反应的离子反应考查,注意离子反应的实质、保留化学式的物质及与量有关的离子反应等,选项D为解答的难点,题目难度不大.

练习册系列答案
相关题目
16.在下列有机物中,能跟溴水发生加成反应,又能被酸性高锰酸钾溶液氧化的是( )
| A. | 乙烯 | B. | 苯 | C. | 甲苯 | D. | 乙烷 |
14.用NA表示阿伏加德罗常数,下列叙述正确的是( )
| A. | 在标准状况下,2.24LH2O中原子数为0.3NA | |
| B. | 0.1mol/L 的NaCl溶液中,Na+与Cl-离子总数为0.2NA | |
| C. | 16g O2和O3的混合气体中含NA个O原子 | |
| D. | 64克铜与足量的硫反应生成硫化铜,理论上会转移2NA个电子 |
1.下列叙述中,正确的是( )
| A. | 含金属元素的离子一定都是阳离子 | |
| B. | 在氧化还原反应中,非金属单质一定是氧化剂 | |
| C. | 金属阳离子被还原不一定得到金属单质 | |
| D. | 某元素从化合态变为游离态时,该元素一定被还原 |
11.四份相同质量的铝与足量下列物质发生反应,能放出氢气且消耗溶质物质的量最少的是( )
| A. | 稀硫酸 | B. | 稀硝酸 | C. | 盐酸 | D. | 氢氧化钠溶液 |
18.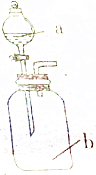 如图所示,将少量试剂a滴入试剂瓶b中,下列实验现象描述正确的是( )
如图所示,将少量试剂a滴入试剂瓶b中,下列实验现象描述正确的是( )
 如图所示,将少量试剂a滴入试剂瓶b中,下列实验现象描述正确的是( )
如图所示,将少量试剂a滴入试剂瓶b中,下列实验现象描述正确的是( )| 选项 | 试剂a | 试剂b | 预测实验现象 |
| A | 浓盐酸 | 二氧化锰 | 产生大量黄绿色气体 |
| B | 烧碱溶液 | 明矾溶液 | 先生成白色沉淀,后溶解 |
| C | 浓硝酸 | 铝片 | 铝片溶解,产生大量红棕色气体 |
| D | 稀硫酸 | 含KSCN的硝酸亚铁溶液 | 溶液变红色,溶液中产生气泡 |
| A. | A | B. | B | C. | C | D. | D |
15.下列实验操作能达到实验目的是( )
| 选项 | 实验操作 | 实验目的 |
| A | 在ZnS的白色浊液中滴几滴CuSO4溶液 | 探究Ksp(ZnS)和Ksp(CuS)的相对大小 |
| B | 用pH试纸分别测定等浓度的NaF、NaClO溶液的pH | 探究HF与HClO的电离常数 |
| C | 取少量硝酸亚铁溶液,滴加盐酸和KSCN溶液 | 探究硝酸亚铁是否变质 |
| D | 在CH2=CHCH2OH中滴加酸性高锰酸钾溶液,振荡 | 检验丙烯醇是否具有碳碳双键 |
| A. | A | B. | B | C. | C | D. | D |
17.以葡萄糖为燃料的微生物燃料电池结构示意图如图,关于该电池的叙述不正确的是( )
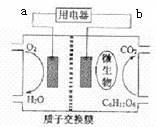

| A. | 微生物促进了反应中电子的转移 | |
| B. | 连接a的电极为负极 | |
| C. | 放电过程中,质子(H+)从负极区向正极区迁移 | |
| D. | 电池的负极反应为:C6H12O6+6H2O-24e-═6CO2+24H+ |