题目内容
湿法脱硝技术可用于处理烟气中的氮氧化物,发生的化学反应为:
2NH3(g)+NO(g)+NO2(g)
2N2(g)+3H2O(g)△H<0
在恒容的密闭容器中,按2:1:1的比例通入NH3、NO、NO2混合气体,平衡时氮氧化物去除率可达80%.下列有关说法正确的是( )
2NH3(g)+NO(g)+NO2(g)
| 180℃ |
| 催化剂 |
在恒容的密闭容器中,按2:1:1的比例通入NH3、NO、NO2混合气体,平衡时氮氧化物去除率可达80%.下列有关说法正确的是( )
| A、若其他条件不变,反应温度改为400℃,能更快达到同样的氮氧化物去除率 |
| B、若其他条件不变,改用高效催化剂,能更快达到同样的氮氧化物去除率 |
| C、平衡时,其他条件不变,再向容器中通入NH3,氮氧化物去除率将高于80% |
| D、平衡时,其他条件不变,再升高温度可使该反应的平衡常数增大 |
考点:化学平衡的影响因素
专题:化学平衡专题
分析:A、依据反应是放热反应和平衡移动原理分析;
B、催化剂改变反应速率不改变化学平衡;
C、增大氨气浓度会提高氮氧化物的转化率;
D、反应是放热反应,升高温度平衡逆向进行.
B、催化剂改变反应速率不改变化学平衡;
C、增大氨气浓度会提高氮氧化物的转化率;
D、反应是放热反应,升高温度平衡逆向进行.
解答:
解:A、反应是放热反应,若其他条件不变,反应温度改为400℃,平衡逆向进行,不能更快达到同样的氮氧化物去除率,故A错误;
B、催化剂改变反应速率不改变化学平衡,若其他条件不变,改用高效催化剂,能更快达到同样的氮氧化物去除率,故B正确;
C、增大氨气浓度会提高氮氧化物的转化率,平衡时,其他条件不变,再向容器中通入NH3,氮氧化物去除率将高于80%,故C正确;
D、反应是放热反应,升高温度平衡逆向进行,平衡常数减小,故D错误;
故选BC.
B、催化剂改变反应速率不改变化学平衡,若其他条件不变,改用高效催化剂,能更快达到同样的氮氧化物去除率,故B正确;
C、增大氨气浓度会提高氮氧化物的转化率,平衡时,其他条件不变,再向容器中通入NH3,氮氧化物去除率将高于80%,故C正确;
D、反应是放热反应,升高温度平衡逆向进行,平衡常数减小,故D错误;
故选BC.
点评:本题考查了化学平衡影响因素分析判断,平衡移动原理的分析应用时关键,题目较简单.

练习册系列答案
相关题目
下列四组等质量的铁与过量的盐酸在不同条件下反应,反应速率由快到慢的顺序排列正确的是( )
| 组别 | c(HCl/mol/L) | 温度/℃ | 状态 |
| 1 | 2.0 | 25 | 块状 |
| 2 | 2.5 | 30 | 块状 |
| 3 | 2.5 | 50 | 粉末状 |
| 4 | 2.5 | 30 | 粉末状 |
| A、4-3-2-1 |
| B、1-2-3-4 |
| C、3-4-2-1 |
| D、1-2-4-3 |
下列分子的空间构型为三角锥形的是( )
| A、CO2 |
| B、NH3 |
| C、CO2 |
| D、BF3 |
在硫酸钠和硫酸钾的混和溶液中,当n(Na+)=0.2mol,n(SO42-)=x mol,n(K+)=y mol时,则x和y的关系是( )
| A、y=2(x+0.1) | ||
B、x=
| ||
| C、y=2x-0.1 | ||
D、x=0.1+
|
下列关于乙醇的说法正确的是( )
| A、乙醇在水溶液中能电离出少量的H+,所以乙醇是电解质 |
| B、乙醇结构中有-OH,所以乙醇显碱性 |
| C、乙醇分子中只有烃基上的氢原子可被钠置换出来 |
| D、乙醇是一种很好的溶剂,能溶解许多无机化合物和有机化合物,人们用白酒浸泡中药制成药酒就是利用了这一性质 |
化学与科学、技术、社会、环境密切相关.下列有关说法中正确的是( )
| A、煤经过气化和液化两个物理变化,可变为清洁能源 |
| B、天宫一号使用的碳纤维是一种新型的有机高分子材料 |
| C、发酵粉中主要含有氢氧化钠,能使焙制出的糕点疏松多孔 |
| D、石油催化裂化的主要目的是提高汽油等轻质油的产量与质量,石油裂解的主要目的是得到更多的乙烯、丙烯等气态短链烃 |
下列物质中,可用来鉴别乙酸溶液,葡萄糖溶液和淀粉溶液的是( )
| A、新制氢氧化铜悬浊液 | B、溴水 |
| C、稀盐酸 | D、碳酸钠溶液 |
下列有机物的系统命名正确的是( )
A、 异丁烷 |
B、 2-甲基-3-丁烯 |
C、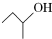 2-丁醇 |
D、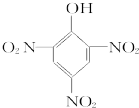 1,3,5-三硝基苯酚 |
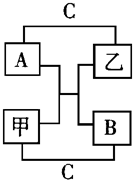 A、B、C是短周期里的3种元素的单质,甲、乙是常见的化合物,它们之间存在如图所示的转化关系:若A为有色气体,C 为无色气体,B为淡黄色固体,请回答:
A、B、C是短周期里的3种元素的单质,甲、乙是常见的化合物,它们之间存在如图所示的转化关系:若A为有色气体,C 为无色气体,B为淡黄色固体,请回答: