题目内容
15.25℃时,50mL 0.10mol•L-1醋酸中存在下述平衡:CH3COOH?CH3COO-+H+,若分别作如下改变,对上述平衡有何影响?①加入少量冰醋酸,平衡将右移,(填“左移”、“右移”)溶液中c(H+)将增大(填“增大”、“减小”或“不变”);
②加入一定量蒸馏水,平衡将右移,(填“左移”、“右移”)溶液中c(H+)将减小(填“增大”、“减小”或“不变”).
分析 ①加入冰醋酸,醋酸浓度增大平衡向正反应方向移动;
②加水稀释促进醋酸电离,但醋酸电离增大程度小于溶液体积增大程度;
解答 解:①加入冰醋酸,醋酸浓度增大平衡向正反应方向移动,电离平衡右移,溶液中C(H+)增大,故答案为:右移;增大;
②加水稀释促进醋酸电离,电离平衡右移,但醋酸电离增大程度小于溶液体积增大程度,C(H+)减小,故答案为:右移;减小;
点评 本题考查弱电解质的电离,明确改变条件对哪种离子浓度影响来分析平衡移动方向,注意影响平衡移动的因素分析判断,掌握基础是解题关键,题目难度不大.

练习册系列答案
 七星图书口算速算天天练系列答案
七星图书口算速算天天练系列答案
相关题目
5.下列表示物质结构的化学用语或模型中,不正确的是( )
| A. | 8个中子的碳原子的核素符号:14C | |
| B. | 碳酸氢钠的电离方程式:NaHCO3=Na++H++CO32- | |
| C. | Cl-离子的结构示意图 | |
| D. | 氯化钠的电子式: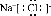 |
6.下列叙述正确的是( )
| A. | 自然界中大量存在硅单质 | |
| B. | 石英、水晶、硅石的主要成分都是SiO2 | |
| C. | 自然界中SiO2都存在于石英矿中 | |
| D. | SiO2为集成电路和光电池的材料 |
3.有甲、乙、丙三种溶液,进行如下操作:

则甲、乙、丙三种溶液可能是( )

则甲、乙、丙三种溶液可能是( )
| A. | BaCl2、H2SO4、MgCl2 | B. | CaCl2、HNO3、BaCl2 | ||
| C. | CaCl2、HNO3、NaCl | D. | BaCl2、HCl、Na2SO4 |
20.下列关于药物使用的说法中,正确的是( )
| A. | 长期大量服用阿司匹林可预防疾病,没有毒副作用 | |
| B. | 碘酒能使蛋白质变性,常用于外敷消毒 | |
| C. | 使用青霉素可直接静脉注射,不需进行皮肤敏感试验 | |
| D. | 随着平价药房的开设,生病了都可以到药店自己买药服用 |
16.在pH=1的无色透明溶液中,能大量共存的离子组是( )
| A. | Al3+、Ag+、NO3-、Cl- | B. | K+、NH4+、NO3-、CO32- | ||
| C. | Fe3+、Ba2+、Cl-、NO3- | D. | Zn2+、Na+、NO3-、SO42- |
 (1)科学家正在研究温室气体CH4和CO2的转化和利用.
(1)科学家正在研究温室气体CH4和CO2的转化和利用.