题目内容
15.在从海带中提取碘的实验中,下列做法错误的是( )| A. | 装有干海带的坩埚置于泥三角上加热灼烧 | |
| B. | 加入过量的氯水确保I-被完全氧化 | |
| C. | 用四氯化碳溶液萃取碘单质,上层为水层可以弃去 | |
| D. | 可利用碘单质易升华的特性来提纯碘单质 |
分析 A.灼烧在坩埚中进行;
B.过量氯水可氧化碘单质;
C.萃取后,四氯化碳在下层;
D.碘易升华.
解答 解:A.灼烧在坩埚中进行,则装有干海带的坩埚置于泥三角上加热灼烧,故A正确;
B.过量氯水可氧化碘单质,则应加适量氯水氧化碘离子,故B错误;
C.碘易溶于四氯化碳,且四氯化碳的密度比水的密度大,则萃取后,四氯化碳在下层,上层为水层可以弃去,故C正确;
D.碘易升华,则利用碘单质易升华的特性来提纯碘单质,故D正确;
故选B.
点评 本题考查海水资源应用及混合物分离提纯,为高频考点,把握物质的性质、性质差异及混合物分离为解答的关键,侧重分析与应用能力的考查,题目难度不大.

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案
相关题目
5.有a、b、c、d四个金属电极,有关的反应装置及部分反应现象如下:
由此可判断这四种金属的活动性顺序是( )
| 实验装置 | 部分实验现象 | 实验装置 | 部分实验现象 |
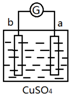 | a极质量减小, b极质量增加 | 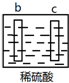 | b极有气体产生, c极无变化 |
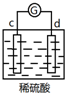 | d极溶解, c极有气体产生 | 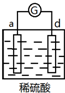 | 电流计指示在导线中电流从a极流向d极 |
| A. | d>a>b>c | B. | b>c>d>a | C. | a>b>c>d | D. | a>b>d>c |
6.下列说法错误的是( )
| A. | 1H和3H是不同的核素 | |
| B. | 1H、2H、3H、H+和H2是氢元素的五种不同粒子 | |
| C. | 12C和14C互为同位素,物理性质不同,但化学性质几乎完全相同 | |
| D. | 石墨和金刚石互为同位素,化学性质相似 |
3.下列有关盐类水解的说法中,正确的是( )
| A. | 所有的盐在水溶液中都能水解 | |
| B. | 盐类水解一定都显酸性或碱性 | |
| C. | 盐类的水解反应是酸碱中和反应的逆反应,因此盐类水解是吸热反应 | |
| D. | 盐类水解抑制了水的电离 |
7.欲分离某CCl4和H2O的混合液,除铁架台、铁圈外,还需要用到的仪器是( )
| A. | 漏斗 | B. | 长颈漏斗 | C. | 分液漏斗 | D. | 直形冷凝管 |
5.现有失去标签的四瓶无色溶液分别为Na2CO3溶液、稀盐酸、Ba(OH)2溶液、NaHSO4溶液,为确定四瓶溶液分别是什么,将其随意标号为A、B、C、D,分别取少量溶液两两混合,产生的现象如下表所示.
已知:NaHSO4属于酸式盐,在水溶液中的电离方程式为:NaHSO4═Na++H++SO42-.
根据实验现象,回答下列问题:
(1)A为Na2CO3溶液,C为稀盐酸.
(2)写出下列反应的离子方程式
A+BCO32-+Ba2+=BaCO3↓,A+DCO32-+2H+=CO2↑+H2O,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为Ba2++OH-+H++SO42-=BaSO4↓+H2O,反应后得到的溶液中含有的阴离子有OH-.
(4)上述没有明显变化的实验④、⑥,其中④发生了离子反应,离子方程式为H++OH-=H2O.请设计实验证明其发生了反应取少量Ba(OH)2溶液滴入几滴酚酞试液,溶液显红色,向该红色溶液中加入稀盐酸至过量,溶液变为无色,说明酸碱发生反应.(试剂任选)
| 实验顺序 | 实验内容 | 实验现象 |
| ① | A+B | 生成白色沉淀 |
| ② | A+C | 放出无色气体 |
| ③ | A+D | 放出无色气体 |
| ④ | B+C | 无明显变化 |
| ⑤ | B+D | 生成白色沉淀 |
| ⑥ | C+D | 无明显变化 |
根据实验现象,回答下列问题:
(1)A为Na2CO3溶液,C为稀盐酸.
(2)写出下列反应的离子方程式
A+BCO32-+Ba2+=BaCO3↓,A+DCO32-+2H+=CO2↑+H2O,
(3)等物质的量浓度、等体积的B、D混合反应的离子方程式为Ba2++OH-+H++SO42-=BaSO4↓+H2O,反应后得到的溶液中含有的阴离子有OH-.
(4)上述没有明显变化的实验④、⑥,其中④发生了离子反应,离子方程式为H++OH-=H2O.请设计实验证明其发生了反应取少量Ba(OH)2溶液滴入几滴酚酞试液,溶液显红色,向该红色溶液中加入稀盐酸至过量,溶液变为无色,说明酸碱发生反应.(试剂任选)