题目内容
4.下列有关金属腐蚀的说法正确的是( )| A. | 金属腐蚀指不纯金属接触到的电解质溶液进行化学反应而损耗的过程 | |
| B. | 电化腐蚀指在外加电流的作用下不纯金属发生化学反应而损耗的过程 | |
| C. | 钢铁腐蚀最普遍的是吸氧腐蚀,负极吸收氧气最终转化为铁锈 | |
| D. | 金属的电化腐蚀和化学腐蚀本质相同,但电化腐蚀伴有电流产生 |
分析 A.金属腐蚀是指金属与周围接触到的空气或液体发生反应而引起损耗的现象;
B.电化学腐蚀是形成原电池,不是外加电流;
C.钢铁吸氧腐蚀是负极铁失电子,氧气在正极上得到电子;
D.依据化学腐蚀和电化腐蚀的实质分析.
解答 解:A.金属腐蚀是指金属与周围接触到的空气或液体发生反应而引起损耗的现象,所以金属的腐蚀不一定接触到电解质溶液,故A错误;
B.电化学腐蚀原理是原电池原理,原电池中不含电源,是自发进行的氧化还原反应,故B错误;
C.钢铁腐蚀最普遍的是吸氧腐蚀,吸氧腐蚀中正极吸收氧气,负极铁失电子最终转化为铁锈,故C错误;
D.金属的电化腐蚀和化学腐蚀都是金属失电子被氧化的反应,本质相同,但电化腐蚀过程中形成的原电池反应会产生微弱的电流,故D正确;
故选D.
点评 本题考查化学腐蚀与电化腐蚀原理及其应用,题目难度不大,金属腐蚀和金属的保护是考试的重点,明确原电池、电解池工作原理为解答关键,注意明确化学腐蚀与电化学腐蚀的实质与区别,试题培养了学生的灵活应用能力.

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
12.已知括号中为杂质,则下列除杂试剂正确的是( )
| A. | 丙烷(丙烯),酸性高锰酸钾溶液 | B. | 甲烷(乙炔),溴的四氯化碳溶液 | ||
| C. | 溴苯(溴),苯 | D. | 硝基苯(硝酸),苯和浓硫酸 |
15.将一定质量的钠铝合金置于水中,合金全部溶解.得到20mLNaOH和NaAlO2的混合溶液,然后用lmol/L的盐酸与之反应.至沉淀量最大时消耗盐酸40mL,则原合金中钠的质量为( )
| A. | 0.92g | B. | 0.69g | C. | 0.46g | D. | 0.23g |
12.金属钛(Ti)被誉为21世纪金属,具有良好的生物相容性,它兼具铁的高强度和铝的低密度.其单质和化合物具有广泛的应用价值.氮化钛(Ti3N4)为金黄色晶体,由于具有令人满意的仿金效果,越来越多地成为黄金的代替品.以TiCl4为原料,经过一系列反应可以制得Ti3N4和纳米TiO2(如图1).
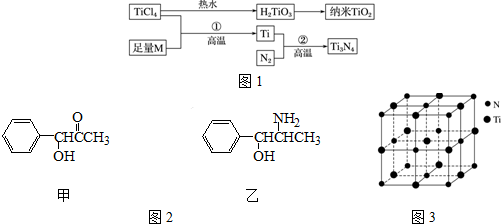
图中的M是短周期金属元素,M的部分电离能如表:请回答下列问题:
(1)Ti的基态原子外围电子排布式为4d25s2;
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
KCl、CaO、TiN三种离子晶体熔点由高到低的顺序为TiN>CaO>KCl.

图中的M是短周期金属元素,M的部分电离能如表:请回答下列问题:
| I1 | I2 | I3 | I4 | I5 | |
| 电离能/kJ•mol-1 | 738 | 1451 | 7733 | 1054 0 | 13630 |
(2)M是Mg(填元素符号),该金属晶体的堆积模型为六方最密堆积,配位数为12;
(3)纳米TiO2是一种应用广泛的催化剂,纳米TiO2催化的一个实例如图2所示.化合物甲的分子中采取sp2方式杂化的碳原子有7个,化合物乙中采取sp3方式杂化的原子对应的元素的电负性由大到小的顺序为O>N>C;
(4)有一种氮化钛晶体的晶胞与NaCl晶胞相似,如图3所示,该晶胞中N、Ti之间的最近距离为a pm,则该氮化钛的密度为$\frac{4×62}{{N}_{A}×(2a×1{0}^{-10})^{3}}$ g•cm-3(NA为阿伏加德罗常数的值,只列计算式).该晶体中与N原子距离相等且最近的N原子有12个;
(5)科学家通过X-射线探明KCl、MgO、CaO、TiN的晶体与NaCl的晶体结构相似.且知三种离子晶体的晶格能数据如下:
| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ•mol-1 | 786 | 715 | 3401 |
19.NA表示阿伏加德罗常数,下列说法正确的是( )
| A. | 32 g氧气和臭氧的混合物含有的原子数为NA | |
| B. | 39 g Na2O2含有2 NA个离子 | |
| C. | 标准状况下,22.4 L 乙醇所含分子数为NA | |
| D. | 18 g D2O含有的分子数为NA |
9.某化学兴趣小组欲研究一种镁铝合金,以下是部分实验.请完成填空.
[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol•L-1NaOH溶液(足量)的锥形瓶里.
(1)从反应开始至反应结束,依次可观察到的现象有:①切口断面处先产生气泡,反应由慢到快;②小块合金在溶液中上下翻腾;③溶液升温;④反应后,溶液中残留黑色固体.
(2)开始时产生气泡速率慢,其主要原因(除温度、电化学因素外)是合金表面有氧化膜.
(3)欲利用此反应测定合金中铝的含量,请仿照方法①写出另一种不同方法所需数据.
[实验二]向实验一的锥形瓶里滴加1mol•L-1HCl,使镁、铝两种元素恰好只以氯化物的形式存在.
[实验三]请设计合理实验检验实验二所得溶液中的Mg2+、Al3+.
限选实验用品与试剂:烧杯、试管、滴管、1mol•L-1NaOH溶液、1mol•L-1HCl溶液、蒸馏水.
根据你设计的实验方案,叙述实验操作、预期现象和结论.(可填满、可不填满)
[实验四]粉末状试样A是由MgO和Fe2O3组成的混合物.取适量A进行铝热反应,产物中有单质B生成.
产物中的单质B是Fe(填化学式).
[实验一]从镁铝合金片上剪下一小块,先称重,然后投到盛有10mL 10mol•L-1NaOH溶液(足量)的锥形瓶里.
(1)从反应开始至反应结束,依次可观察到的现象有:①切口断面处先产生气泡,反应由慢到快;②小块合金在溶液中上下翻腾;③溶液升温;④反应后,溶液中残留黑色固体.
(2)开始时产生气泡速率慢,其主要原因(除温度、电化学因素外)是合金表面有氧化膜.
(3)欲利用此反应测定合金中铝的含量,请仿照方法①写出另一种不同方法所需数据.
| 方法 | 需测定的数据 |
| ① | 测定产生的H2的体积 |
| ② | “测定残留固体镁的质量”或“测定反应消耗或剩余的NaOH的量”或“测定生成的NaAlO2的量” |
[实验三]请设计合理实验检验实验二所得溶液中的Mg2+、Al3+.
限选实验用品与试剂:烧杯、试管、滴管、1mol•L-1NaOH溶液、1mol•L-1HCl溶液、蒸馏水.
根据你设计的实验方案,叙述实验操作、预期现象和结论.(可填满、可不填满)
| 实验操作 | 预期现象和结论 |
| 步骤1: | |
| 步骤2: | |
| … |
产物中的单质B是Fe(填化学式).
16.把Cu粉放入稀硫酸,加热后并无明显现象,当加入一种盐的晶体后,可看到溶液呈蓝色,同时有气体逸出,此盐晶体是( )
| A. | FeCl3 | B. | Na2SO4 | C. | Na2CO3 | D. | NaNO3 |
13.锂电池是新一代的高能电池,它以质轻、能高而受到普遍重视.目前已经研制成功了多种锂电池.某种锂电池的总反应可表示为:Li+MnO2═LiMnO2,若该电池提供5C电荷量(其他损耗忽略不计),则消耗的正极材料的质量约为(式量Li:7,MnO2:87,电子电荷量取1.60×10-19 C)( )
| A. | 3.5×10-3 g | B. | 7×10-4 g | C. | 4.52×10-3 g | D. | 4.52×10-2 g |
14.已知在酸性条件下有以下反应关系:
(1)KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2.
(2)Br2能将I-氧化为I2.
(3)KIO3能将I-氧化为I2,也能将Br-氧化为Br2,其本身被还原为I2.
①上述物质中氧化剂氧化能力由强到弱的顺序是KBrO3>KIO3>Br2.
②现向含有1molKI的硫酸溶液中加入含amolKBrO3的溶液,a的取值范围不同,所得产物也不同.试将讨论的结果填入下表.
③若产物中碘单质和碘酸钾的物质的量相等,a的值为$\frac{8}{15}$.
④若a的值为1时,其产物及其物质的量分别为I2:0.1mol、KIO3:0.8mol、Br2:0.5mol.
(1)KBrO3能将KI氧化成I2或KIO3,其本身被还原为Br2.
(2)Br2能将I-氧化为I2.
(3)KIO3能将I-氧化为I2,也能将Br-氧化为Br2,其本身被还原为I2.
①上述物质中氧化剂氧化能力由强到弱的顺序是KBrO3>KIO3>Br2.
②现向含有1molKI的硫酸溶液中加入含amolKBrO3的溶液,a的取值范围不同,所得产物也不同.试将讨论的结果填入下表.
| 编号 | a的取值范围 | 产物的化学式或(离子符号) |
| A | a≤$\frac{1}{6}$ | I2,Br- |
| B | $\frac{1}{6}$<a<$\frac{1}{5}$ | I2、Br-、Br2 |
| C | a=$\frac{1}{5}$ | I2、Br2 |
| D | $\frac{1}{5}$<a<$\frac{6}{5}$ | I2,IO3-,Br2 |
| E | a≥$\frac{6}{5}$ | IO3-、Br2 |
④若a的值为1时,其产物及其物质的量分别为I2:0.1mol、KIO3:0.8mol、Br2:0.5mol.