题目内容
 如图表示一个电解池,装有电解质溶液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:
如图表示一个电解池,装有电解质溶液a;X、Y是两块电极板,通过导线与直流电源相连.请回答以下问题:(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则
①Y电极上的电极反应式
②在X电极附近观察到的现象是
(2)若X、Y都是惰性电极,a是浓度均为2mol?L-1的AgNO3与Cu(NO3)2的混合溶液1L,电解一段时间后,X电极上有3.2g铜析出,写出电解过程中有关反应的离子方程式
(3)如果要用电解的方法精炼粗铜(含有Fe、Zn、Pt、C等杂质),电解质溶液a选用CuSO4溶液,则:
①X电极的材料是
②精炼完成后,硫酸铜溶液的浓度
(4)铅蓄电池反应的化学方程式是Pb+PbO2+2H2SO4=2PbSO4+2H2O.若以铅蓄电池为电源,用惰性电极电解CuSO4溶液,在电解过程中生成11.2LO2(标准状况),则铅蓄电池中消耗的硫酸的物质的量为
考点:电解原理
专题:
分析:(1)电解饱和食盐水时,阳极上是氯离子失电子,阴极上是氢离子得电子,氯气能使湿润的碘化钾淀粉试纸变蓝;
(2)若X、Y都是铜电极,a是浓度均为2mol?L-1的AgNO3与Cu(NO3)2的混合溶液1L,阳极反应为Cu2++2e-=Cu,阴极首先析出银,然后析出铜;
(3)电解方法精炼粗铜,电解液a选用CuSO4溶液,粗铜做阳极,精铜做阴极,结合电极反应判断;
(4)用惰性电极电解CuSO4溶液,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,n(O2)=
=0.5mol,根据电子守恒计算;
(2)若X、Y都是铜电极,a是浓度均为2mol?L-1的AgNO3与Cu(NO3)2的混合溶液1L,阳极反应为Cu2++2e-=Cu,阴极首先析出银,然后析出铜;
(3)电解方法精炼粗铜,电解液a选用CuSO4溶液,粗铜做阳极,精铜做阴极,结合电极反应判断;
(4)用惰性电极电解CuSO4溶液,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,n(O2)=
| 11.2L |
| 22.4L/mol |
解答:
解:(1)①和电源的正极相连的电极Y极是阳极,该电极上氯离子发生失电子的氧化反应,即2Cl--2e-=Cl2↑,故答案为:2Cl--2e-=Cl2↑;
②和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,故答案为:放出气体,溶液变红;
(2)由于氧化性Ag+>Cu2+,阳极首先发生Ag++e-=Ag,然后发生Cu2++2e-=Cu,所以电解过程中有关反应的离子方程式4Ag++2H2O
4Ag+O2↑+4H+,2Cu2++2H2O
2Cu+O2↑+4H+,电解一段时间后X电极上有3.2g铜析出,说明Ag已经全被析出,共转移电子应为n(Ag+)+2n(Cu2+)=2mol+
×2=2.1mol,
故答案为:4Ag++2H2O
4Ag+O2↑+4H+,2Cu2++2H2O
2Cu+O2↑+4H+,2.1;
(3)①电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu2++2e-=Cu,故答案为:纯铜; Cu2++2e-=Cu;
②精炼粗铜(含有Fe、Zn、Pt、C等杂质),阳极为粗铜先是锌、铁失电子生成离子,而阴极是溶液中的铜离子得电子析出铜单质,则硫酸铜溶液的浓度变小,故答案为:变小;
(4)用惰性电极电解CuSO4溶液,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,n(O2)=
=0.5mol,转移0.5mol×4=2mol电子,由方程式可知Pb+PbO2+2H2SO4=2PbSO4+2H2O,消耗2mol硫酸,故答案为:2mol.
②和电源的负极相连的电极X极是阴极,该电极上氢离子发生得电子的还原反应,即2H++2e-=H2↑,所以该电极附近氢氧根浓度增大,碱性增强,滴入几滴酚酞试液会变红,故答案为:放出气体,溶液变红;
(2)由于氧化性Ag+>Cu2+,阳极首先发生Ag++e-=Ag,然后发生Cu2++2e-=Cu,所以电解过程中有关反应的离子方程式4Ag++2H2O
| ||
| ||
| 3.2g |
| 64g/mol |
故答案为:4Ag++2H2O
| ||
| ||
(3)①电解方法精炼粗铜,电解池的阴极材料是纯铜,电极反应为:Cu2++2e-=Cu,故答案为:纯铜; Cu2++2e-=Cu;
②精炼粗铜(含有Fe、Zn、Pt、C等杂质),阳极为粗铜先是锌、铁失电子生成离子,而阴极是溶液中的铜离子得电子析出铜单质,则硫酸铜溶液的浓度变小,故答案为:变小;
(4)用惰性电极电解CuSO4溶液,在阳极上是氢氧根离子放电,电极反应式为:4OH--4e-=2H2O+O2↑,n(O2)=
| 11.2L |
| 22.4L/mol |
点评:本题考查了电解原理的分析应用,主要是电极反应和电极判断,电子守恒是电化学计算的依据,掌握基础是关键,题目较简单.

练习册系列答案
相关题目
用惰性电极电解下列物质的水溶液,一段时间后(温度不变),再加入一定质量的另一种物质(括号内物质),溶液能恢复到与电解前的溶液完全一样的是( )
| A、CuCl2(CuO) |
| B、NaOH(Na2O) |
| C、NaCl(NaCl) |
| D、H2SO4(H2O) |
 如图曲线表示在2L密闭容器中,反应aX(g)?bY(g)+cZ(g)中各物质的物质的量随时间变化的关系,则该反应的化学方程式为( )
如图曲线表示在2L密闭容器中,反应aX(g)?bY(g)+cZ(g)中各物质的物质的量随时间变化的关系,则该反应的化学方程式为( )| A、X?Y+Z |
| B、X?2Y+Z |
| C、2X?2Y+Z |
| D、2X?4Y+Z |
下列说法正确的是( )


| A、与铜质水龙头连接处的钢质水管不易发生腐蚀 |
| B、用电解法提取氯化铜废液中的铜,可以用碳棒连接电源的正极,另一电极用铜片 |
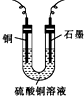
| C、图1中,接通开关时Zn腐蚀速率增大,Zn上放出气体的速率也增大 |
| D、图2所示装置可发生反应的离子方程式为Zn+2H+=Zn2++H2↑,且a、b电极不可能是同种材料 |
 当pH为4~5时,Cu2+几乎不水解,而Fe3+几乎完全沉淀.某同学欲用电解纯净CuSO4溶液的方法来测定铜的相对原子质量.实验过程中使用肼(N2H4)-空气燃料电池作直流电源,其实验过程如图所示:
当pH为4~5时,Cu2+几乎不水解,而Fe3+几乎完全沉淀.某同学欲用电解纯净CuSO4溶液的方法来测定铜的相对原子质量.实验过程中使用肼(N2H4)-空气燃料电池作直流电源,其实验过程如图所示: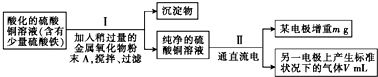
 某温度下,将三种气体充入一密闭容器中,所发生反应的平衡常数可表示为K=
某温度下,将三种气体充入一密闭容器中,所发生反应的平衡常数可表示为K=