题目内容
5.我国科研人员以Zn和尖晶石百锰酸锂(ZnMn2O4)为电极材料,研制出一种水系锌离子电池.该电池的总反应方程式:xZn+Zn1-xMn2O4$?_{充电}^{放电}$ZnMn2O4(0<x<1).下列说法正确的是( )| A. | ZnMn2O4是负极材料 | |
| B. | 充电时,Zn2+向ZnMn2O4电极迁移 | |
| C. | 充电时,阳极反应:ZnMn2O4-xZn2+-2xe-=Zn1-x Mn2O4 | |
| D. | 充放电过程中,只有Zn元素的化合价发生变化 |
分析 A、锌失电子发生氧化反应;
B、电解池阳离子向阴极移动;
C、电解池中阳极发生氧化反应;
D、放电时锰元素的化合价降低.
解答 解:A、锌失电子发生氧化反应,所以锌是负极材料,故A错误;
B、电解池阳离子向阴极移动,而可充可放电池中,阴极是原电池的负极,所以Zn2+向锌迁移,故B错误;
C、电解池中阳极发生氧化反应,所以阳极的电极反应为:ZnMn2O4-xZn2+-2xe-=Zn1-x Mn2O4,故C正确;
D、放电时锰元素的化合价降低,所以放电时锌与锰的化合价变化,故D错误;
故选C.
点评 本题考查了原电池和电解池原理,根据元素化合价变化确定各个电极上发生的反应,难点是电极反应式的书写,题目难度中等.

练习册系列答案
相关题目
15.下列反应中,SO2作为氧化剂而发生反应的是( )
| A. | 2SO2+O2═2SO3 | B. | SO2+H2O═H2SO3 | ||
| C. | SO2+2H2S═3S↓+2H2O | D. | SO2+Cl2+2H2O═H2SO4+2HCl |
16.下列物质不能用于鉴别碳酸钠和碳酸氢钠溶液的是( )
| A. | 稀盐酸 | B. | 氢氧化钡溶液 | C. | 氯化钙溶液 | D. | 硫酸氢钠溶液 |
13.化学与生产、生活密切相关,下列说法正确的是( )
| A. | 煤的干馏可得煤油、石蜡和沥青 | |
| B. | 工业上以氯气和石灰乳为原料制备漂白粉 | |
| C. | 干燥剂硅胶和硅橡胶的主要成分都是二氧化硅 | |
| D. | 二氧化硫有漂白性,常用作棉、麻和食品的漂白 |
5.A~E是中学常见的5种化合物,A、B是氧化物,它们之间的转化关系如图所示.则下列说法正确的是( )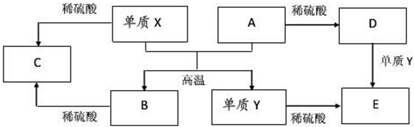

| A. | 单质X与A反应的化学方程式:Al2O3+2Fe$\frac{\underline{\;高温\;}}{\;}$Fe2O3+2Al | |
| B. | 检验D溶液中金属阳离子的反应:Fe3++3SCN-=Fe(SCN)3↓ | |
| C. | 单质X和单质Y在一定条件下均能与水发生置换反应 | |
| D. | 由于化合物B和C均既能与酸反应,又能与碱反应,所以两者均是两性氧化物 |
12.下列有关化学用语的表示正确的是( )
| A. | Ne和Na+的结构示意图均为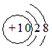 | |
| B. | NaHCO3在水中的电离方程式为NaHCO3=Na++HCO3- | |
| C. | 聚氯乙烯的结构简式为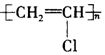 | |
| D. | MgCl2的电子式为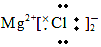 |



