题目内容
12.为了测定K2CO3和NaHCO3混合物的组成,某学生每次称取一定质量的混合物溶于水配成溶液,向其中加入相同浓度的Ba(OH)2溶液,每次实验均充分反应,实验结果记录如表:| 实验次数 | 混合物的质量/g | 所加Ba(OH)2溶液的体积/L | 测得沉淀的质量/g |
| 1 | 1.716 | 0.5 | 2.758 |
| 2 | 3.432 | 0.5 | |
| 3 | 5.148 | 0.5 | 8.274 |
| 4 | 6.864 | 0.5 | 11.032 |
| 5 | 8.580 | 0.5 | 11.032 |
| 6 | 10.296 | 0.5 | 11.032 |
(1)第二次实验中产生沉淀的质量是5.516g;
(2)求所用Ba(OH)2的溶液的物质的量浓度0.112 g•mol-1;
(3)求混合物中K2CO3和NaHCO3的物质的量之比5:2;
(4)在25℃时,取下第3组实验所得溶液体积的$\frac{1}{10}$,加水配成1000mL溶液,求此溶液pH=12.
分析 (1)根据第1次与第2次样品之比等于沉淀质量之比,据此计算第2次生成沉淀的质量;
(2)实验中每次滴加相同浓度的Ba(OH)2溶液500mL,第4次、第5次、第6次生成沉淀碳酸钡质量都为11.032g,说明样品质量为6.864g时,氢氧化钡已经完全反应,碳酸钡的物质的量为$\frac{11.032g}{197g/mol}$=0.056mol,根据钡离子守恒可知氢氧化钡的物质的量为0.056mol,据此计算;
(3)第3次实验中样品完全反应,令碳酸氢钠与碳酸钾的物质的量分别为xmol、ymol,根据碳元素守恒可知沉淀碳酸钡的物质的量为(x+y)mol,根据样品质量与碳酸钡沉淀质量列方程计算;
(4)第3组实验,反应后溶液为氢氧化钡、氢氧化钠、氢氧化钾的混合溶液,由钡离子守恒计算n[Ba(OH)2],根据钠离子、钾离子守恒计算n(NaOH)、n(KOH),进而计算溶液的$\frac{1}{10}$中含有n(OH-),再根据c=$\frac{n}{v}$计算,故c(H+)=$\frac{kw}{c(O{H}^{-})}$,并据pH=-lgc(H+)进行计算.
解答 解:(1)第2次实验中样品完全反应,设产生沉淀质量为mg,则1.716g:3.432g=2.758:mg,解得m=5.516,
故答案为:5.516;
(2)实验中每次滴加相同浓度的Ba(OH)2溶液500mL,第3次、第4次生成沉淀碳酸钡质量都为5.516g,说明样品质量为3.342g时,氢氧化钡已经完全反应,碳酸钡的物质的量为$\frac{11.032g}{197g/mol}$=0.056mol,根据钡离子守恒可知氢氧化钡的物质的量为0.056mol,所以Ba(OH)2溶液中溶质的物质的量浓度是$\frac{0.056mol}{0.5L}$=0.112mol/L,
故答案为:0.112;
(3)第3次实验中样品完全反应,设碳酸氢钠与碳酸钾的物质的量分别为xmol、ymol,根据碳元素守恒可知沉淀碳酸钡的物质的量为:(x+y)mol,则:84x+138y=5.148g、197x+197y=8.274,
解得:x=0.012,y=0.03,
故样品中K2CO3和NaHCO3的物质的量之比为0.03mol:0.012mol=5:2,
故答案为:5:2;
(4)第3组实验,反应后溶液为氢氧化钡、氢氧化钠、氢氧化钾的混合溶液,由钡离子守恒:n[Ba(OH)2]=0.056mol-$\frac{8.274g}{197g/mol}$=0.014mol,根据钠离子守恒:n(NaOH)=n(NaHCO3)=0.012mol,根据钾离子守恒:n(KOH)=2n(K2CO3)=0.03mol×2=0.06mol,所以溶液中n总(OH-)=2n[Ba(OH)2]+n(NaOH)+n(KOH)=0.014mol×2+0.012mol+0.06mol=0.1mol,取所得溶液体积的$\frac{1}{10}$,含有的氢氧根的物质的量为0.01mol,加水配成1000mL溶液,c(OH-)=$\frac{0.01mol}{1L}$=0.01mol/L,故c(H+)=$\frac{kw}{c(O{H}^{-})}$=$\frac{1{0}^{-14}}{0.01}$=10-12,pH=-lgc(H+)=-lg10-12=12,
故答案为:12.
点评 本题考查混合物的计算、实验数据分析处理等,综合性较大,根据质量定比关系判断过量问题是解题关键,旨在考查学生的综合能力,是一道不错的能力考查题,题目难度较大.

 长江作业本同步练习册系列答案
长江作业本同步练习册系列答案(1)实验室可通过反应2Na2S+Na2CO3+4SO2→3Na2S2O3+CO2制取Na2S2O3,装置如图所示.
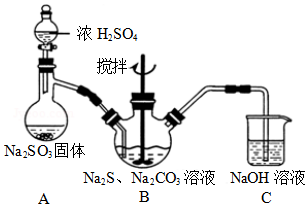
装置B中搅拌器的作用是让反应物充分反应(或反应物充分混合或加快反应速度);装置C中NaOH溶液的作用是吸收二氧化硫尾气,防止空气污染.
(2)请对上述装置提出一条优化措施A中分液漏斗改为恒压漏斗(或者BC之间添加一个安全瓶防倒吸).
为测定所得保险粉样品中Na2S2O3•5H2O的质量分数,称取3.000g Na2S2O3•5H2O样品配成100mL溶液,用0.100mol/L标准碘溶液进行滴定,反应方程式为:2Na2S2O3+I2→2NaI+Na2S4O6
(3)滴定时用淀粉作指示剂,滴定时使用的主要玻璃仪器有滴定管、锥形瓶.
(5)滴定时,若看到溶液局部变色就停止滴定,则样品中Na2S2O3•5H2O的质量分数测定值偏低(填“偏高”、“偏低”或“不变”).
(5)某学生小组测得实验数据如表:
| 实验次数 | 样品溶液体积(mL) | 滴定消耗0.100mol/L碘溶液体积(mL) |
| 1 | 20.00 | 9.80 |
| 2 | 20.00 | 10.70 |
| 3 | 20.00 | 9.90 |
| A. | 500mL | B. | 500L | C. | 1L | D. | 无法求解 |
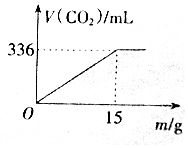 一定质量的铁碳合金在足量的氧气中燃烧,合金质量与生存二氧化碳体积(已换算为标准状况)关系如图所示,则此铁碳合金是( )
一定质量的铁碳合金在足量的氧气中燃烧,合金质量与生存二氧化碳体积(已换算为标准状况)关系如图所示,则此铁碳合金是( )| A. | 低碳钢 | B. | 中碳钢 | C. | 高碳钢 | D. | 合金钢 |
| A. | 碘是人体内必须的微量元素,所以富含高碘酸的食物适合于所有人群 | |
| B. | 化石燃料不完全燃烧会产生CO造成污染,完全燃烧不会造成大气污染 | |
| C. | 利用铁比铜金属性强的性质,常用FeCl3溶液腐蚀Cu来刻制印刷电路板 | |
| D. | 中国古代利用明矾溶液清除铜镜表面的铜镑,是利用了明矾溶液的酸性 |