题目内容
12.下列说法正确的是( )| A. | 40K和40Ca原子中的质子数和中子数都相等 | |
| B. | 任何元素的原子都是由核外电子和核内中子、质子组成的 | |
| C. | 具有相同核电荷数的粒子,一定是同种原子的微粒 | |
| D. | 同种元素的不同核素之间互为同位素 |
分析 A、元素符号的左下角数字表示质子数,左上角数字表示质量数,中子数=质量数-质子数;
B、氢元素的一种原子:氕,是不含有中子的原子;
C、有相同核电荷数的粒子,如F-、0H-;
D、质子数相同而中子数不同的同一元素的不同原子互称同位素.
解答 解:A、40K中质子数是19,中子数是21;40Ca中质子数是20,中子数是20,故A错误;
B、氕的质子数为1,中子数为0,是不含有中子的原子,故B错误;
C、具有相同核电荷数的粒子,不一定是同种原子的微粒,如F-、0H-,故C错误;
D、同种元素的不同核素,质子数相同,中子数不同,它们之间互为同位素,故D正确.
故选D.
点评 本题考查了原子的构成、同位素的性质等知识点,注意举例说明.

练习册系列答案
 课堂全解字词句段篇章系列答案
课堂全解字词句段篇章系列答案 步步高口算题卡系列答案
步步高口算题卡系列答案 点睛新教材全能解读系列答案
点睛新教材全能解读系列答案
相关题目
2.将体积均为10mL、pH均为3的盐酸和醋酸,加入水稀释至amL和bmL,测得稀释后溶液的pH均为5,则稀释后溶液的体积( )
| A. | a=b=100 | B. | a=b=1000 | C. | a<b | D. | a>b |
3.下列关于气体摩尔体积的叙述正确的是( )
| A. | 1 mol任何气体的体积都为22.4 L | |
| B. | 1 mol任何物质在标准状况下所占的体积都为22.4 L | |
| C. | 标准状况下,1 mol四氯化碳所占的体积是22.4 L | |
| D. | 标准状况下,22.4 L的任何气体的物质的量都是1 mol |
20.当光束通过下列分散系时,不可能产生丁达尔效应的是( )
| A. | 墨水 | B. | Fe(OH)3胶体 | C. | CuSO4溶液 | D. | 稀豆浆 |
7.下列各组混合物中,以任意比例混合,只要总质量固定,经充分燃烧后产生CO2的量为一恒定值的是( )
| A. | 甲烷和乙烷 | B. | 乙醇和乙酸 | C. | 丙烯和丙烷 | D. | 乙炔和苯蒸气 |
17.几种短周期元素的原子半径及主要化合价如表:
下列叙述正确的是( )
| 元素代号 | X | Y | Z | W |
| 原子半径/pm | 160 | 143 | 70 | 66 |
| 主要化合价 | +2 | +3 | +3、+5、-3 | -2 |
| A. | X、Y元素的金属性X<Y | |
| B. | Y的最高价氧化物对应的水化物能溶于稀氨水 | |
| C. | 一定条件下,W单质可以将Z从其氢化物中置换出来 | |
| D. | 常温下,Z单质与W的常见单质直接生成2W2 |
4.绿色化学是将反应物全部转化为期望的产物,使原子的利用率达到100%,以减少有害物质生成的化学工艺理念.下列符合“绿色化学”要求的是( )
| A. | 湿法冶铜:Fe+CuSO4═FeSO4+Cu | |
| B. | 高炉炼铁:Fe2O3+3CO═2Fe+3CO2 | |
| C. | 制氧气:2KMnO4$\frac{\underline{\;\;△\;\;}}{\;}$K2MnO4+MnO2+O2↑ | |
| D. | 制环氧乙烷:2C2H2( 乙炔)+O2$\frac{\underline{\;催化剂\;}}{加热}$2C2H4O ( 环氧乙烷) |
1.如图所示是四种分子结构的排列方式,其对应的化学式正确的是( )
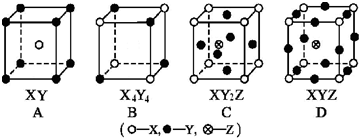

| A. | A | B. | B | C. | C | D. | D |
2.下列说法错误的是( )
| A. | I的原子半径大于Br,HI比HBr的热稳定性强 | |
| B. | P的非金属性强于Si,H3PO4比H2SiO3的酸性强 | |
| C. | 锂所在周期元素最高价氧化物对应的水化物中,酸性最强的是HNO3 | |
| D. | 常压下,0℃时冰的密度比水的密度小,水在4℃时密度最大,这些都与氢键有关 |