题目内容
下列物质的电离方程式,不正确的是( )
| A、NaClO=Na++ClO- |
| B、H2CO3?2H++CO32- |
| C、NaHSO4═H++SO42-+Na+ |
| D、Al2(SO4)3=2Al3++3SO42- |
考点:电离方程式的书写
专题:电离平衡与溶液的pH专题
分析:用化学式和离子符号表示电离过程的式子,称为电离方程式,电离方程式中,离子所带电荷数一般可根据它们在化合物中的化合价来判断,所有阳离子带的正电荷总数与所有阴离子所带的负电荷总数相等,离子团不能拆开.弱电解质的电离用“?”,强电解质的电离用“═”,以此来解答.
A.次氯酸钠完全电离出钠离子和次氯酸根离子;
B.多元弱酸应分步电离;
C.硫酸氢钠,完全电离电离出钠离子和氢离子和硫酸根离子;
D.Al2(SO4)3为强电解质完全电离出铝离子和硫酸根离子.
A.次氯酸钠完全电离出钠离子和次氯酸根离子;
B.多元弱酸应分步电离;
C.硫酸氢钠,完全电离电离出钠离子和氢离子和硫酸根离子;
D.Al2(SO4)3为强电解质完全电离出铝离子和硫酸根离子.
解答:
解:A.次氯酸钠为强电解质,完全电离出钠离子和次氯酸根离子NaClO=Na++ClO-,故A正确;
B.H2CO3为多元弱酸,分步电离,则电离方程式为H2CO3?H++HCO3-、HCO3-?H++CO32-,故B错误;
C.NaHSO4是强电解质,NaHSO4在水中电离出钠离子和硫酸根离子和氢离子,NaHSO4═Na++H++SO42-,故C正确;
D.Al2(SO4)3为强电解质完全电离,Al2(SO4)3═2Al3++3SO42-,电离方程式书写正确,故D正确;
故选B.
B.H2CO3为多元弱酸,分步电离,则电离方程式为H2CO3?H++HCO3-、HCO3-?H++CO32-,故B错误;
C.NaHSO4是强电解质,NaHSO4在水中电离出钠离子和硫酸根离子和氢离子,NaHSO4═Na++H++SO42-,故C正确;
D.Al2(SO4)3为强电解质完全电离,Al2(SO4)3═2Al3++3SO42-,电离方程式书写正确,故D正确;
故选B.
点评:本题考查电离方程式的书写知识,注意强电解质在溶液中能完全电离,弱电解质部分电离,离子团在电离方程式中不能拆开,强酸的酸式根离子要拆开,弱酸的酸式根离子不能拆开,碳酸电离为该题易错点,题目难度不大.

练习册系列答案
 学练快车道快乐假期寒假作业系列答案
学练快车道快乐假期寒假作业系列答案
相关题目
深秋及寒冬的清晨,我们安庆市经常出现大雾天气,雾中小液滴直径范围是( )
| A、小于1 nm |
| B、在1~100 nm间 |
| C、大于100 nm |
| D、无法确定 |
下列说法或表示方法正确的是( )
A、丙烷分子的比例模型: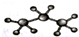 |
| B、乙醚的分子式为:C2H6O |
C、2-乙基-1,3-丁二烯分子的键线式: |
| D、化学名词:乙酸乙脂、苯、活性碳、钳锅 |
常温下pH=6的盐酸和pH=6的NH4Cl溶液,其中由水电离出的c(H+)分别为x mol/L、y mol/L,则x与y的关系是( )
| A、x=10-2y |
| B、x>y |
| C、x=y |
| D、x=102y |
根据下表中烃的分子式排列规律,空格中烃的同分异构体中一氯代物种数不可能是( )
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 |
| CH4 | C2H4 | C3H8 | C4H8 | C6H12 | C7H16 | C8H16 |
| A、1种 | B、2种 | C、3种 | D、4种 |
下列分离、提纯、鉴别物质的方法正确的是( )
| A、用加热、蒸发的方法可以除去粗盐中的CaCl2、MgCl2杂质 |
| B、用渗析的方法除去NaCl溶液中含有的少量淀粉胶体 |
| C、用溶解、过滤的方法提纯含有少量BaSO4的BaCO3 |
| D、用丁达尔效应鉴别Fe(OH)3胶体和FeCl3溶液 |
下列反应的离子方程式正确的是( )
| A、氨气通入醋酸溶液CH3COOH+NH3═CH3COONH4 |
| B、金属钠跟水反应Na+H2O═Na++OH-+H2↑ |
| C、碳酸钡溶于醋酸BaCO3+2H+═Ba2++H2O+CO2↑ |
| D、澄清的石灰水跟盐酸反应H++OH-═H2O |
下列叙述中,正确的是( )
| A、在氧化还原反应中,肯定有一种元素被氧化,另一种元素被还原 |
| B、得电子越多的氧化剂,其氧化性就越强 |
| C、反应前各原子的物质的量之和一定等于反应后各原子的物质的量之和 |
| D、溶液稀释前溶质的物质的量一定等于溶液稀释后溶质的物质的量 |