题目内容
17.下列有关甲烷的说法不正确的是( )| A. | 甲烷分子中四个碳氢键键长相等 | |
| B. | 甲烷分子中四个碳氢键键角相等 | |
| C. | 甲烷分子中四个碳氢键键能相等 | |
| D. | 由于甲烷分子三个键参数都分别相等,所以甲烷的空间构型是平面正方形结构 |
分析 甲烷的中心原子是碳原子,碳原子上的价电子都形成了共价键,中心原子价层孤电子对数$\frac{4+1×4}{2}$=4,碳原子sp3杂化,该分子是正四面体结构;甲烷分子中只有C-H键的键能、键长和键角完全相同,据此进行解答.
解答 解:A.甲烷为正四面体结构,四个碳氢键完全相同,则四个碳氢键键长相等,故A正确;
B.甲烷分子为正四面体结构,其分子中四个碳氢键键角相等,故B正确;
C.甲烷分子为正四面体结构,四个碳氢键键能相等,故C正确;
D.甲烷的中心原子是碳原子,碳原子上的价电子都形成了共价键,中心原子价层孤电子对数$\frac{4+1×4}{2}$=4,碳原子sp3杂化,该分子是正四面体结构,故D错误;
故选D.
点评 本题考查有机物结构判断,题目难度不大,明确甲烷分子构型为解答关键,注意掌握常见有机物组成、结构与性质,试题培养了学生的灵活应用能力.

练习册系列答案
相关题目
8.实验室制备1,2-二溴乙烷的反应原理如下:CH3CH2OH$→_{170℃}^{浓硫酸}$CH2=CH2↑+H2O,CH2=CH2+Br2→BrCH2CH2Br.用少量的溴和足量的乙醇制备1,2-二溴乙烷的装置如图所示:

有关数据列表如下:
回答下列问题:
(1)在装置C中应加入c(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水②浓硫酸③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是溴的颜色完全褪去.
(3)若产物中有少量未反应的Br2,最好用②(填正确选项前的序号)洗涤除去.
①水②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(4)反应过程中需用冷水冷却(装置e),其主要目的是避免溴的大量挥发;但不用冰水进行过度冷却,原因是:1,2-二溴乙烷的凝固点较低,过度冷却会使其凝固而使气路堵塞.
(5)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2-二溴乙烷通过消去反应制得乙炔,反应的化学方程式为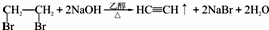 ;乙炔制得氯乙烯;最后由氯乙烯制得氯乙烯,反应的化学方程式为nCH2=CHCl$\stackrel{一定条件}{→}$
;乙炔制得氯乙烯;最后由氯乙烯制得氯乙烯,反应的化学方程式为nCH2=CHCl$\stackrel{一定条件}{→}$ .
.

有关数据列表如下:
| 乙醇 | 1,2-二溴乙烷 | 乙醚 | |
| 状态 | 无色液体 | 无色液体 | 无色液体 |
| 密度/g•cm-3 | 0.79 | 2.2 | 0.71 |
| 沸点/℃ | 78.5 | 132 | 34.6 |
| 熔点/℃ | -130 | 9 | -116 |
(1)在装置C中应加入c(选填序号),其目的是吸收反应中可能生成的酸性气体.
①水②浓硫酸③氢氧化钠溶液 ④饱和碳酸氢钠溶液
(2)判断d管中制备二溴乙烷反应已结束的最简单方法是溴的颜色完全褪去.
(3)若产物中有少量未反应的Br2,最好用②(填正确选项前的序号)洗涤除去.
①水②氢氧化钠溶液 ③碘化钠溶液 ④乙醇
(4)反应过程中需用冷水冷却(装置e),其主要目的是避免溴的大量挥发;但不用冰水进行过度冷却,原因是:1,2-二溴乙烷的凝固点较低,过度冷却会使其凝固而使气路堵塞.
(5)以1,2-二溴乙烷为原料,制备聚氯乙烯,为了提高原料利用率,有同学设计了如下流程:1,2-二溴乙烷通过消去反应制得乙炔,反应的化学方程式为
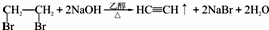 ;乙炔制得氯乙烯;最后由氯乙烯制得氯乙烯,反应的化学方程式为nCH2=CHCl$\stackrel{一定条件}{→}$
;乙炔制得氯乙烯;最后由氯乙烯制得氯乙烯,反应的化学方程式为nCH2=CHCl$\stackrel{一定条件}{→}$ .
.
5.有4种碳架如下的烃,下列说法正确的是( )


| A. | a和b互为同分异构体 | B. | b和c是同系物 | ||
| C. | a和b都能发生加成反应 | D. | 只有b和c能发生取代反应 |
12. 室温下,用0.100mol•L-1的NaOH溶液分别滴定均为20.00mL0.100mol•L-1的HCl溶液和醋酸溶液,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1的NaOH溶液分别滴定均为20.00mL0.100mol•L-1的HCl溶液和醋酸溶液,滴定曲线如图所示.下列说法正确的是( )
 室温下,用0.100mol•L-1的NaOH溶液分别滴定均为20.00mL0.100mol•L-1的HCl溶液和醋酸溶液,滴定曲线如图所示.下列说法正确的是( )
室温下,用0.100mol•L-1的NaOH溶液分别滴定均为20.00mL0.100mol•L-1的HCl溶液和醋酸溶液,滴定曲线如图所示.下列说法正确的是( )| A. | I表示的是滴定醋酸的曲线 | |
| B. | pH=7时,滴定醋酸消耗的V(NaOH)>20.00mL | |
| C. | V(NaOH)=20.00mL时,两份溶液中c(Cl-)>c(CH3COO-) | |
| D. | V(NaOH)=10.00mL时,醋酸中c(Na+)>c(CH3COO-)>c(H+)>c(OH-) |


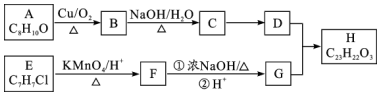
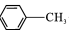 $\stackrel{KMnO_{4}/H+}{→}$
$\stackrel{KMnO_{4}/H+}{→}$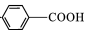
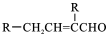
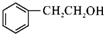 ,C→D的反应类型为加成反应;B中含氧官能团名称为醛基,F中不含氧的官能团的名称为氯原子; H的结构简式为
,C→D的反应类型为加成反应;B中含氧官能团名称为醛基,F中不含氧的官能团的名称为氯原子; H的结构简式为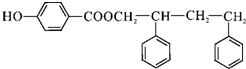 ;
;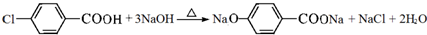 ;
;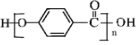 ;
;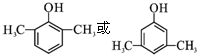 .
.
 已知X、Y、Z、M、G是五种短周期主族元素,且原子序数依次增大.X原子核内只有1个质子,Y的原子最外层电子数是其电子层数的2倍,Y与G同主族,Z的一种单质能吸收对人体有害的紫外线,M是地壳中含量最高的金属元素.请回答下列问题:
已知X、Y、Z、M、G是五种短周期主族元素,且原子序数依次增大.X原子核内只有1个质子,Y的原子最外层电子数是其电子层数的2倍,Y与G同主族,Z的一种单质能吸收对人体有害的紫外线,M是地壳中含量最高的金属元素.请回答下列问题: