题目内容
1.在4L的密闭容器中,充入1mol N2和4mol H2,在一定条件下反应,3分钟后达到平衡状态,相同温度下,测得平衡时气体的压强比反应前混合气体的压强减少了12%,请计算:(1)平衡时混合气体中三种气体的物质的量之比为n(N2):n(H2):n(NH3)=7:31:6
(2)N2的转化率为30%
(3)3分钟内NH3的平均反应速率为0.05mol/(L•min).
分析 令参加反应的氮气的物质的量为nmol,根据三段式解题法,表示出反应混合物各组分物质的量的变化量、平衡时各组分的物质的量.
(1)根据压强之比等于物质的量之比,列方程求出n的值,进而确定三种气体的物质的量之比;
(2)根据转化率的定义计算,转化率=$\frac{消耗量}{起始量}$×100%;
(3)根据v=$\frac{△c}{△t}$计算v(NH3).
解答 解:根据三段式解题法,表示出反应混合物各组分物质的量的变化量、平衡时各组分的物质的量.
令参加反应的氮气的物质的量为nmol,则:
N2 +3H2 ?2NH3 ,
开始(mol):1 4 0
变化(mol):n 3n 2n
平衡(mol):1-n 4-3n 2n
压强之比等于物质的量之比,所以(1-n+4-3n+2n)mol=(1+4)mol×(1-12%),解得n=0.3,
(1)平衡时n(N2)=(1-n)mol=(1-0.3)mol=0.7mol
平衡时n(H2)=(4-3n)mol=(4-3×0.3)mol=3.1mol
平衡时n(NH3)=2n=0.3mol×2=0.6mol
所以n(N2):n(H2):n(NH3)=0.7mol:3.1mol:0.6mol=7:31:6,
故答案为:n(N2):n(H2):n(NH3)=7:31:6;
(2)N2 的转化率为$\frac{0.3mol}{1mol}$×100%=30%,
故答案为:30%;
(3)3分钟内,以H2 表示的平均反应速率v(NH3)=$\frac{\frac{0.6mol}{4L}}{3min}$=0.05 mol/(L•min),
故答案为:0.05 mol/(L•min).
点评 本题考查化学平衡的有关计算,主要是反应速率,转化率等概念的理解应用,难度不大,注意基础知识的掌握与三段式解题法的运用.

 巧学巧练系列答案
巧学巧练系列答案| A. | 甲中反应达到平衡时,Q1=Q | |
| B. | 达到平衡后,甲中C的体积分数比乙大 | |
| C. | 达到平衡后,再向乙中加入0.25molA、0.75molB、1.5molC,平衡向生成C的方向移动 | |
| D. | 乙中的热化学反应方程式为2C(g)?A(g)+3B(g)△H=+Q2kJ/mol |
| 阳离子 | K+、Al3+、Ba2+、NH4+ |
| 阴离子 | Cl-、OH-、SO42-、CO32- |
(1)Cl-离子的结构示意图是
 . Al3+、K+、SO42-三种离子可组成一种盐,写出该盐的一种用途净水剂.
. Al3+、K+、SO42-三种离子可组成一种盐,写出该盐的一种用途净水剂.(2)将含OH-离子的溶液 滴入浓度均为0.1 mol/L的Al3+和NH4+的混合溶液中,若测得溶液中NH4+减少了一半,此时,溶液中不存在(填“存在”或“不存在”)大量的Al3+.
(3)物质A和B分别由上表中的两种离子组成,将它们分别溶于水中,A的溶液显酸性,将A、B两溶液混合,微热,既有白色沉淀,又有使湿润的红色石蕊试纸变蓝的气体生成.
则B的阳离子是Ba2+,用离子方程式表示A溶液显酸性的原因NH4++H2O
 NH3•H2O+H+.
NH3•H2O+H+.(4)常温下,将(NH4)2CO3溶于水,得到含有大量NH4+和CO32-的溶液,往溶液中滴入少量氨水,测得溶液中N H4+和CO32 -的浓度比为2:1,此时该溶液的pH<( 填“<”、“=”或“>”)7.
(5)在微生物作用的条件下,NH4+可被空气氧化成NO3-.写出该反应的离子方程式:NH4++2O2=NO3-+H2O+2H+.
(6)在一个固定容积为5L的密闭容器中充入0.10mol N2和0.30molH2,一定条件下,半分钟后达到平衡,测得容器中含NH3 0.08mol,则ν(H2)=0.048mol.L-1.min-1,此时N2的转化率为40%;若继续通入0.10mol N2和0.30molH2,则平衡向正反应方向移动(填“向正反应方向”、“向逆反应方向”或“不”).
| T/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
(1)该反应的化学平衡常数表达式为K=$\frac{c(CO)×c({H}_{2}O)}{c(C{O}_{2})×c({H}_{2})}$
(2)该反应为吸热反应(填“吸热”或“放热”).
(3)某温度下,各物质的平衡浓度符合下式:3c(CO2)•c(H2)=5c(CO)•c(H2O),试判断此时的温度 为700℃
(4)若830℃时,向容器中充入1mol CO、5mol H2O,反应达到平衡后,其化学平衡常数 K等于1.0(填“大于”“小于”或“等于”).
(5)830℃时,容器中的反应已达到平衡.在其他条件不变的情况下,扩大容器的体积,平衡不移动(填“向正反应方向”“向逆反应方向”或“不”).
(6)若1200℃时,在某时刻平衡体系中CO2、H2、CO、H2O的浓度分别为2mol/L、2mol/L、4mol/L、4mol/L,则此时上述反应的平衡移动方向为逆反应方向(填“正反应方向”“逆反应方向”或“不移动”)
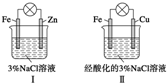
| A. | Ⅰ中不能形成原电池 | |
| B. | Ⅱ中负极反应是Fe-3e-═Fe3+ | |
| C. | Ⅱ中正极反应是O2+2H2O+4e-═4OH- | |
| D. | Ⅱ中加入少量K3[Fe(CN)6]溶液,有蓝色沉淀 |
| A. | 氢氧化铁溶胶、水玻璃、淀粉溶液、PM2.5微粒均具有丁达尔效应 | |
| B. | 明矾和漂白粉常用于自来水的处理,两者的作用原理相同 | |
| C. | 氯化铁溶液可用于制作印刷电路板是因为其具有较强氧化性,与铜发生置换反应 | |
| D. | 高温能杀死流感病毒是因为构成病毒的蛋白质受热变性 |
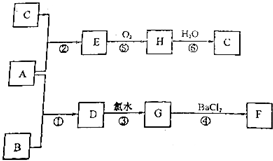
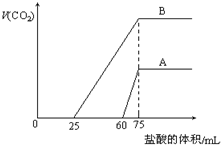 取来两份等浓度的NaOH溶液A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题:
取来两份等浓度的NaOH溶液A和B,每份10mL,分别向A、B中通入不等量的CO2,再继续向两溶液中逐滴加入0.2mol/L的盐酸,标准状况下产生的CO2气体体积与所加的盐酸溶液体积之间的关系如图所示,试回答下列问题: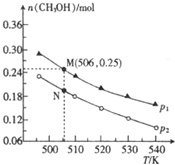 以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.
以天然气为原料合成甲醇常见的方法有水煤气法和目前正在开发的直接氧化法.