题目内容
19.物质的量浓度相同的下列溶液,pH由大到小排列正确的是( )| A. | Ba(OH)2、Na2SO3、FeCl3、KCl | B. | Na2CO3、NaHCO3、KNO3、NH4Cl | ||
| C. | NH3•H2O、H3PO4、Na2SO4、H2SO4 | D. | NaCl、CH3COOH、AlCl3、NaHSO4、 |
分析 根据碱溶液的pH>盐溶液的pH>酸溶液的pH,及盐溶液中强酸弱碱盐水解显酸性、强碱弱酸盐水解显碱性、不水解的盐显中性、盐中有弱才水解、越弱越水解等来解答.
解答 解:A、pH由大到小排列为:Ba(OH)2、Na2SO3、KCl、FeCl3,氯化铁显示酸性,亚硫酸钠具有碱性,二者都是因为存在的弱离子水解的原因,故A错误;
B、碳酸根离子水解程度大于碳酸氢根离子,所以碳酸钠碱性强于碳酸氢钠,硝酸钾显示中性,氯化铵显示酸性,所以pH大小顺序是:Na2CO3、NaHCO3、KNO3、NH4Cl,故B正确;
C、硫酸钠显示中性,磷酸显示酸性,溶液的pH大小顺序是:NH3•H2O、Na2SO4、H3PO4、H2SO4,故C错误;
D、氯化铝水解显示酸性,醋酸属于酸显示酸性,醋酸的酸性要强,所以pH大小顺序是:NaCl、AlCl3、CH3COOH、NaHSO4,故D错误.
故选B.
点评 本题考查盐类水解的原理及应用,侧重于学生的分析能力可基本理论知识的综合运用的考查,注意把握盐类水解的原理以及影响因素,难度不大.

练习册系列答案
 习题精选系列答案
习题精选系列答案
相关题目
7.在试管中注入某红色溶液,给试管加热,溶液颜色逐渐变浅,则原溶液可能是( )
①滴有石蕊试液的碳酸 ②滴有石蕊试液的NH4Cl溶液
③滴有石蕊试液的硫酸 ④滴有酚酞试液的氨水
⑤滴有酚酞试液的氢氧化钠溶液 ⑥滴有酚酞试液的饱和氢氧化钙溶液
⑦滴有酚酞试液的Na2CO3溶液 ⑧溶有SO2的品红溶液.
①滴有石蕊试液的碳酸 ②滴有石蕊试液的NH4Cl溶液
③滴有石蕊试液的硫酸 ④滴有酚酞试液的氨水
⑤滴有酚酞试液的氢氧化钠溶液 ⑥滴有酚酞试液的饱和氢氧化钙溶液
⑦滴有酚酞试液的Na2CO3溶液 ⑧溶有SO2的品红溶液.
| A. | ①②④⑥ | B. | ④⑥ | C. | ③⑤⑦⑧ | D. | ②④⑥⑧ |
14.下列既属于无机物,又属于碱的是( )
| A. | Na2CO3 | B. | CH4 | C. | CH3CH2OH | D. | Cu(OH)2 |
9.表是元素周期表的一部分,针对①~⑩种元素,请回答有关问题:
(1)表中化学性质最不活泼的元素,其原子结构示意图为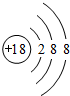 .
.
(2)写出⑤和⑨两种元素的最高价氧化物对应的水化物相互反应的化学方程式Al(OH)3+KOH=KAlO2+2H2O.
(3)用电子式表示④元素与⑦元素形成化合物的过程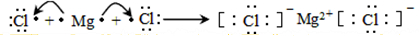 .
.
(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)①、⑦两元素形成的化合物电子式是 ,该化合物分子内含有极性键(填“极性”或“非极性”).
,该化合物分子内含有极性键(填“极性”或“非极性”).
(6)可以证明⑦的单质比⑩的单质氧化性强的离子反应方程式为2Br-+Cl2=Br2+2Cl-.
| 周期 主族 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ③ | |||||
| 3 | ④ | ⑤ | ⑥ | ⑦ | ⑧ | |||
| 4 | ⑨ | ⑩ |
 .
.(2)写出⑤和⑨两种元素的最高价氧化物对应的水化物相互反应的化学方程式Al(OH)3+KOH=KAlO2+2H2O.
(3)用电子式表示④元素与⑦元素形成化合物的过程
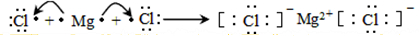 .
.(4)①、②、⑥、⑦四种元素的最高价氧化物的水化物中酸性最强的是HClO4(填化学式).
(5)①、⑦两元素形成的化合物电子式是
 ,该化合物分子内含有极性键(填“极性”或“非极性”).
,该化合物分子内含有极性键(填“极性”或“非极性”).(6)可以证明⑦的单质比⑩的单质氧化性强的离子反应方程式为2Br-+Cl2=Br2+2Cl-.
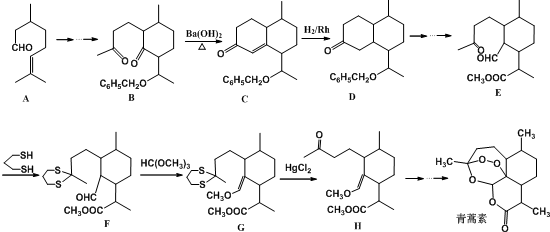
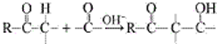
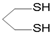 用系统命名法命名,它的名称是1,3-丙二硫醇;
用系统命名法命名,它的名称是1,3-丙二硫醇; 是一种具有菠萝气味的食用香料,是化合物甲与苯氧乙酸
是一种具有菠萝气味的食用香料,是化合物甲与苯氧乙酸 发生酯化反应的产物.
发生酯化反应的产物. $\stackrel{一定条件下}{→}$
$\stackrel{一定条件下}{→}$ .
.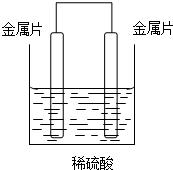 现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡;②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应;③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.装置如图所示,根据上述情况,回答下列问题:
现有A、B、C、D四种金属片,①把A、B用导线连接后同时浸入稀硫酸中,A上有气泡;②把C、D用导线连接后同时浸入稀硫酸中,D发生还原反应;③把A、C用导线连接后同时浸入稀硫酸中,电子流动方向为A→导线→C.装置如图所示,根据上述情况,回答下列问题: