题目内容
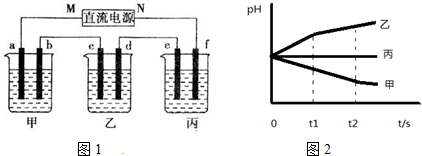
17.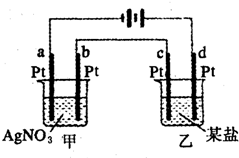 如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.64g某金属,下列说法正确的是( )
如图所示的装置,两烧杯中均为相应的水溶液,通电一段时间后,测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.64g某金属,下列说法正确的是( )| A. | 甲池是b极上析出金属银,乙池是c极上析出某金属 | |
| B. | 甲池是a极上析出金属银,乙池是d极上析出某金属 | |
| C. | 某盐溶液可能是CuSO4溶液 | |
| D. | 某盐溶液可能是Mg(NO3)2溶液 |
分析 测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.24g某金属,甲中a为阴极,b为阳极,银在a极析出,乙中c为阴极,d为阳极,金属在c极析出,乙池电极析出0.64g金属,说明乙池中含有氧化性比氢离子强的金属,以此解答该题.
解答 解:测得甲池中某电极质量增加2.16g,乙池中某电极上析出0.64g某金属,甲中a为阴极,b为阳极,银在a极析出,乙中c为阴极,d为阳极,金属在c极析出,
A、甲池a极上析出金属银,乙池c极上析出某金属,故A错误;
B、甲池a极上析出金属银,乙池c极上析出某金属,故B错误;
C、乙池电极析出0.64g金属,说明乙池中含有氧化性比氢离子强的金属,则某盐溶液可能是CuSO4溶液,故C正确;
D、Mg2+氧化性较弱,电解时在溶液中不能得电子析出金属,所以某盐溶液不能是Mg(NO3)2溶液,故D错误;
故选C.
点评 本题考查了电解池的工作原理,侧重于电解原理的考查,注意把握阴阳极的判断以及溶液离子的放电顺序,题目难度不大.

练习册系列答案
相关题目
12.某有机物A的分子式为C4HxCly,其中x+y=10,已知该有机物有9种同分异构体(不考虑立体异构),则X可能为:①2,②3,③8,④10.下列组合正确的是( )
| A. | ①③ | B. | ①② | C. | ②③ | D. | ②④ |
2.铁可以形成多种氧化物、氢氧化物和盐类.铁与二氧化碳、水在某一密闭体系中反应情况如下表所示:
完成下列填空:
(1)反应Ⅰ是吸热(选填“吸热”,“放热”)反应.根据反应Ⅰ与Ⅱ可以推导出同温下K1、K2与K3之间的关系,则K3=$\frac{{K}_{2}}{{K}_{1}}$(用K1、K2表示).
(2)973K时,若反应Ⅲ在一个容积为2L的反应容器内2min时达到平衡,有3mol电子发生转移,则在2min内v(CO2)=0.375mol•(L•s)-1.若压缩容器的容积为原来的一半,平衡将不移动(选填“向左”,“向右”,“不”),CO2的浓度将增大(选填“增大”,“减小”,“不变”).使该反应的平衡转化率及平衡常数都增大的措施有降低温度.
| 化学反应 | 平衡常数 | 温度 | |
| 973K | 1173K | ||
| ⅠFe(s)+CO2(g)=FeO(s)+CO(g) | K1 | 1.47 | 2.15 |
| ⅡFe(s)+H2O(g)=FeO(s)+H2(g) | K2 | 2.38 | 1.67 |
| ⅢCO(g)+H2O(g)=CO2(g)+H2(g) | K3 | ? | ? |
(1)反应Ⅰ是吸热(选填“吸热”,“放热”)反应.根据反应Ⅰ与Ⅱ可以推导出同温下K1、K2与K3之间的关系,则K3=$\frac{{K}_{2}}{{K}_{1}}$(用K1、K2表示).
(2)973K时,若反应Ⅲ在一个容积为2L的反应容器内2min时达到平衡,有3mol电子发生转移,则在2min内v(CO2)=0.375mol•(L•s)-1.若压缩容器的容积为原来的一半,平衡将不移动(选填“向左”,“向右”,“不”),CO2的浓度将增大(选填“增大”,“减小”,“不变”).使该反应的平衡转化率及平衡常数都增大的措施有降低温度.
9.如图所表示的反应是吸热反应的是( )
| A. | 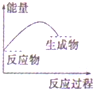 | B. | 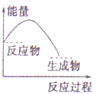 | C. | 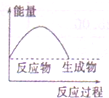 | D. | 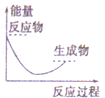 |
7.下列对分子及其性质的解释中,不正确的是( )
| A. | 碘易溶于四氯化碳,甲烷难溶于水都可用相似相溶原理解释 | |
| B. | 乳酸[CH3CH(OH)COOH]中存在一个手性碳原子 | |
| C. | 许多过渡金属离子对多种配体具有很强的结合力,因而,只有过渡金属才能形成配合物 | |
| D. | 已知酸性:H3PO4>HClO,是因为H3PO4分子中有1个非羟基氧原子为0 |
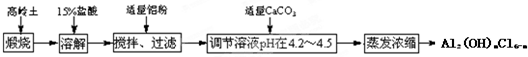
 2C,在反应过程中C的物质的量分数随温度变化如图所示:
2C,在反应过程中C的物质的量分数随温度变化如图所示: