题目内容
ClO2是一种杀菌消毒效率高、二次污染小的水处理剂。实验室中可通过以下反应制得ClO2:2KClO3+H2C2O4+H2SO4 = 2ClO2↑+K2SO4+2CO2↑+2H2O,下列说法不正确的是
A.CO2是氧化产物
B.H2C2O4在反应中被氧化
C.1mol KClO3参加反应,转移的电子为1mol
D.H2C2O4的氧化性强于ClO2的氧化性
D
【解析】
试题分析:A.在反应中草酸中的C的化合价为+3价,反应后变为CO2中的+4价,化合价升高,失去电子,因此CO2是氧化产物,正确;B.在反应中H2C2O4中的C的化合价升高,失去电子,被氧化,作还原剂,正确;C.由于在反应中只有KClO3的Cl的化合价由反应前的+5价变为反应后的+4价,化合价降低1价,所以1mol KClO3参加反应,转移的电子为1mol,正确;D.根据氧化还原反应的规律:还原性:还原剂>还原产物,可得H2C2O4的还原性强于ClO2的还原性,错误。
考点:考查氧化还原反应中物质的性质、作用及电子转移的知识。

练习册系列答案
相关题目
根据下列实验现象,所得结论错误的是
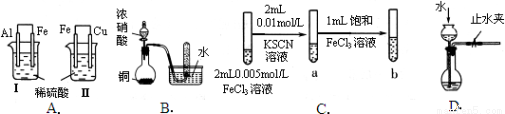
实验 | 实验现象 | 结论 |
A | Ⅰ烧杯中铁片表面有气泡,Ⅱ烧杯中铜片表面有气泡 | 活动性:Al>Fe>Cu |
B | 试管中收集到无色气体 | 铜与浓硝酸反应产物是NO |
C | 试管b比试管a中溶液的红色深 | 增大反应物浓度,平衡向正反应方向移动 |
D | 长颈漏斗内液面高于烧瓶内液面且保持不变 | 装置气密性良好 |
 O,2Fe3++H2O2=2Fe2++O2↑+2H+ 下列说法正确的是
O,2Fe3++H2O2=2Fe2++O2↑+2H+ 下列说法正确的是
