题目内容
16.下列各种冶炼方法中可以制得相应金属的是( )| A. | 加热氧化铝 | B. | 加热碳酸钙 | ||
| C. | 电解熔融氯化钠 | D. | 氯化钠与铝粉高温共热 |
分析 金属的冶炼方法有电解法、热还原法、热分解法等,电解法:冶炼活泼金属K、Ca、Na、Mg、Al,一般用电解熔融的氯化物(Al是电解熔融的三氧化二铝)制得;热还原法:冶炼较不活泼的金属Zn、Fe、Sn、Pb、Cu,常用还原剂有(C、CO、H2等);热分解法:Hg、Ag用加热分解氧化物的方法制得,物理分离法:Pt、Au用物理分离的方法制得.
解答 解:A.Al一般用电解熔融的三氧化二铝制得,加热氧化铝,不能制取金属铝,故A错误;
B.钙是活泼金属,可以采用电解熔融氯化钙的方法来获得,高温煅烧碳酸钙得到的是氧化钙和二氧化碳,不能制取金属钙,故B错误;
C.钠是活泼金属,可以采用电解熔融氯化钠的方法来获得金属钠,故C正确;
D.钠的活泼性大于铝,所以不能用铝热反应制取钠,故D错误;
故选C.
点评 本题考查了金属的冶炼方法,金属的活泼性不一样,金属的冶炼方法也是不一样的,可以根据金属活泼性选择合适的冶炼方法,难度不大.

练习册系列答案
 能力评价系列答案
能力评价系列答案 唐印文化课时测评系列答案
唐印文化课时测评系列答案
相关题目
6.下列分子中,中心原子杂化轨道类型相同,分子的空间构型也相同的是( )
| A. | BeCl2、CO2 | B. | H2O、SO2 | C. | SO2、CH4 | D. | NF3、CH2O |
7.球墨铸铁中含有一种铁碳化合物X.实验室测定化合物X的组成实验如下:
化合物18.0g$→_{高温煅烧}^{足量空气}$固体1$\stackrel{过量盐酸}{→}$溶液甲$\stackrel{足量Cl_{2}}{→}$溶液乙$→_{灼烧}^{加热、蒸发}$固体24.0g
下列说法不正确的是( )
化合物18.0g$→_{高温煅烧}^{足量空气}$固体1$\stackrel{过量盐酸}{→}$溶液甲$\stackrel{足量Cl_{2}}{→}$溶液乙$→_{灼烧}^{加热、蒸发}$固体24.0g
下列说法不正确的是( )
| A. | 固体2是氧化铁 | |
| B. | X的化学式可以表示为Fe3C2 | |
| C. | 溶液甲中可能含有Fe3+ | |
| D. | X与足量的热浓硝酸反应有NO2和CO2生成 |
4. 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,△S=+133.7J•(K•mol) -1该反应能否自发进行与温度 有关.
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数
①实验2中以υ(CO2) 表示的平均反应速率为0.16mol•(L•min)-1.900℃是该反应的平衡常数0.17.
②该反应为吸热(填“吸”或“放”)热反应
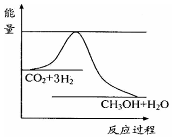
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c (CH3OH)增大的是cd.
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来 d.再充入1mol CO2和3mol H2.
 煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.
煤化工是以煤为原料,经过化学加工使煤转化为气体、液体、固体燃料以及各种化工产品的工业过程.(1)将水蒸气通过红热的碳即可产生水煤气.反应为:C(s)+H2O(g)?CO(g)+H2(g)△H=+131.3kJ•mol-1,△S=+133.7J•(K•mol) -1该反应能否自发进行与温度 有关.
(2)将不同量的CO(g)和H2O(g)分别通入到体积为2L的恒容密闭容器中,进行反应CO(g)+H2O(g)?CO2(g)+H2(g),得到如表三组数
| 实验组 | 温度/℃ | 起始量/mol | 平衡量/mol | 达到平衡所 需时间/min | ||
| H2O | CO | H2 | CO2 | |||
| 1 | 650 | 2 | 4 | 1.6 | 2.4 | 5 |
| 2 | 900 | 1 | 2 | 0.4 | 1.6 | 3 |
②该反应为吸热(填“吸”或“放”)热反应
(3)目前工业上有一种方法是用CO2来生产甲醇.一定条件下发生反应:CO2(g)+3H2(g)?CH3OH(g)+H2O(g),如图表示该反应进行过程中能量(单位为kJ•mol-1)的变化.在体积为1L的恒容密闭容器中,充入1mol CO2和3mol H2,下列措施中能使c (CH3OH)增大的是cd.
a.升高温度 b.充入He(g),使体系压强增大
c.将H2O(g)从体系中分离出来 d.再充入1mol CO2和3mol H2.
11.下列说法正确的是( )
| A. | pH=6的降雨是酸雨 | |
| B. | 氯气泄漏后应顺风向低处跑 | |
| C. | SO2和HClO都具有漂白性,两者的漂白原理相同 | |
| D. | 我国城市环境中的大气污染物主要有SO2、NO2、可吸入颗粒物等 |
1.下列各组物质与其用途的关系不正确的是( )
| A. | 过氧化钠:供氧剂 | B. | 碱石灰:干燥剂 | ||
| C. | 小苏打:发酵粉主要成分 | D. | 纯碱:治疗胃酸过多的一种药剂 |
8.短周期主族元素X、Y、Z、W、M的原子序数依次增大,其中X与其它元素均不位于同一主族,Y和W的原子序数相差8,Y、Z、W三种原子的最外层电子数之和为16,X、Z的最高正价和最低负价的代数和均为0.下列说法正确的是( )
| A. | M的氢化物的水溶液能与W的钠盐溶液,反应得到W的氢化物,说明非金属性M>W | |
| B. | X和Y形成的原子个数比为1:1的分子中极性键和非极性键之比为2:1 | |
| C. | Z元素在自然界中存在游离态 | |
| D. | 原子半径的大小顺序:r(W)>r(Z)>r(Y) |
5.下列有关物质的性质或该物质性质的应用均正确的是( )
| A. | 醋酸与醋酸钠溶液中的醋酸根均可以水解,同浓度时前者的水解程度比后者低一些 | |
| B. | 明矾净水与自来水的杀菌清毒原理是相同的 | |
| C. | MgO和Al2O3常用于制作耐高温材料,工业上采用电解此两种物质冶炼镁、铝金属 | |
| D. | 氯化亚铁溶液加热蒸干并灼烧得到三氧化二铁 |
6.根据图回答,下列说法错误的是( )
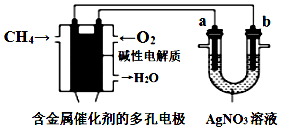

| A. | 电子经导线流入b电极 | |
| B. | 若b极增重5.4 g时,燃料电池负极消耗CH4的体积为140 mL | |
| C. | 燃料电池中正极反应为O2+4e-+2H2O═4OH- | |
| D. | 此装置用于电镀银时,一段时间后硝酸银溶液的浓度不变 |