题目内容
【化学——选修3:物质结构与性质】(15分)过渡金属元素铁能形成多种配合物,如:K3[Fe(SCN)6] [硫氰合铁(Ⅲ)酸钾]和Fe(CO)x等。
(1)①基态Fe3+的M层电子排布式为 。
②请解释+3价铁的化合物较+2价铁的化合物稳定的原因 。
(2)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,则 x = 。
(3)FeBr2为只含有离子键的离子化合物,其晶胞结构如图a,距一个Fe2+离子最近的所有Br-离子为顶点构成的几何体为 。
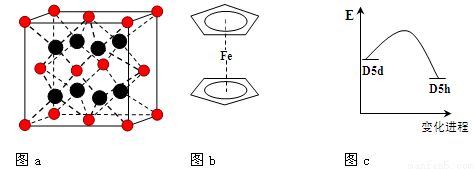
(4)二茂铁是最重要的金属茂基配合物,也是最早被发现的夹心配合物,包含两个环戊二烯基与铁原子成键。二茂铁的结构为一个铁原子处在两个平行的环戊二烯基环的之间,结构如图b所示,已知二茂铁的一氯代物只有一种。
①二茂铁的分子式为 。
②穆斯堡尔谱学数据显示,二茂铁中心铁原子的氧化态为+2,每个茂环带有一个单位负电荷。因此每个环含有 个π电子。
③二茂铁中两个茂环可以是重叠的(D5h),也可以是错位的(D5d),它们之间的能垒仅有8 ~ 20 kJ/mol。温度升高时则绕垂直轴相对转动,使得两种结构可以相互转换,转换过程中能量变化如图c。比较稳定的
是 结构(填“重叠”或“错位”)。
(1)① 3s23p63d5 (2分) ②+3价铁3d轨道有5个电子,处于半充满状态较稳定(2分)
(2)5 (3分) (3)立方体(2分) (4)① C10H10Fe(2分) ② 6(2分) ③ 重叠(2分)
【解析】
试题分析:(1)①铁的原子序数是26,则根据核外电子排布规律可知基态Fe3+的M层电子排布式为3s23p63d5。
②根据铁离子的核外电子排布可知+3价铁3d轨道有5个电子,处于半充满状态较稳定,所以+3价铁的化合物较+2价铁的化合物稳定。
(2)配合物Fe(CO)x的中心原子价电子数与配体提供电子数之和为18,其中中心原子是铁,其价电子数是8,每个配体提供的电子数是2,则8+2x=18,解得 x =5。
(3)根据晶胞结构可知黑球表示溴离子,红球表示亚铁离子,则以面心处的亚铁离子为中心,周围含有8个溴离子,所以距一个Fe2+离子最近的所有Br-离子为顶点构成的几何体为立方体。
(4)①二茂铁的结构为一个铁原子处在两个平行的环戊二烯基环的之间,因此根据环戊二烯基环的化学式C5H5-可知二茂铁的分子式为C10H10Fe。
②二茂铁中心铁原子的氧化态为+2,每个茂环带有一个单位负电荷,因此每个环含有6个π电子。
③能量越低越稳定,根据图像可知重叠的(D5h)能量低,稳定性强。
考点:考查物质与结构性质的分析与应用

 100分闯关期末冲刺系列答案
100分闯关期末冲刺系列答案在学习中,我们经常应用类推法。下列左边正确,类推法应用于右边也正确的是
AA | 向FeCl2溶液中滴入氯水 2Fe2+ + Cl2 = 2Fe3+ + 2Cl— | 向FeCl2溶液中滴入碘水 2Fe2+ + I2 = 2Fe3++2I— |
B | CO2通入漂白粉溶液中 CO2+ Ca2++2ClO—+H2O=CaCO3↓+ 2HClO | SO2通入漂白粉溶液中 SO2 +Ca2++2ClO—+H2O=CaSO3↓+2HClO |
C | 向Na2CO3溶液中滴入稀HNO3 CO32— + 2H+ = CO2↑+ H2O | 向Na2SO3溶液中滴入稀HNO3 SO32— +2H+ = SO2↑+H2O |
D | 向澄清石灰水中通入少量CO2 气体 Ca2++2OH— +CO2 = CaCO3↓+ H2O | 向澄清石灰水中通入少量SO2 气体 Ca2++2OH— +SO2 = CaSO3↓+H2O |


 AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
AX5(g)在容积为10 L的密闭容器中进行。起始时AX3和X2均为0.2 mol。反应在不同条件下进行,反应体系总压强随时间的变化如图所示。
 CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是
CuSO4(s)+5H2O(l),热效应为△H3。则下列判断正确的是